Introduction
Materials and Methods
시료 제조
게놈 DNA 추출 및 polymerase chain reaction (PCR) 검정
제초제저항성 국화의 목적 단백질 발현 분석
물벼룩(Daphnia magna) 배양 조건
물벼룩에 대한 시료 처리 조건
물벼룩 급성 독성 시험 조사 및 평가 항목
Results and Discussion
제초제저항성 국화의 유전자 도입 유전자 검정
시료처리용 시험용수의 수질변화 검정
제초제저항성 국화와 non-GM국화의 처리 농도별 물벼룩의 유영저해 변화
제초제저항성 국화와 non-GM국화의 급이에 의한 물벼룩에 대한 급성독성
Conclusion
Introduction
국화(Chrysanthemum morifolium Ramat.)는 화훼시장에서 장미 다음으로 시장 규모가 큰 화훼류이며 일본에서는 장미나 백합보다 판매량이 많은 화훼작물이다(Aida et al., 2005). 또한 국내에서도 국화의 재배 면적과 생산액이 국내 1 - 2위를 차지하고 있어 주요 화훼작물이라 할 수 있다. 주요 화훼작물인 국화의 품종육성은 현재까지 주로 교배육종을 이용하고 있다(Kang et al., 2011). 이에 반해, 네덜란드와 같은 화훼 선진국에서는 돌연변이 육종과 교배 육종을 통한 신품종 개발이 주로 민간 기업을 통해 이루어지고 있다(Lee et al., 2013). 전 세계적으로 절화와 화분식물의 시장은 항상 꽃색, 화형, 병저항성 등 특이하고 유용한 형질을 가진 품종을 찾고 있다. 이러한 특징 갖는 품종 개발이 전통 교배 육종으로 어려운 경우 생명공학적 접근이 필요하다.
2023년 기준 세계적으로 GM (genetically modified)작물의 재배 면적이 약 2억 6백 30만 헥타르를 기록하였고(Agbioinvestor, 2024), 국내에서는 식품용, 사료용 유전자변형생물체가 약 1,028만 톤이 수입 승인되었고 유전자변형생물체가 약 34.2억 달러의 수입금액을 기록하였다(KBCH, 2024). GM작물의 환경방출 및 실용화를 위해, GM작물에 도입된 유전자들에 대한 환경위해성 평가, 영양 성분 분석과 독성 평가의 안전성 평가가 필수적으로 이루어져야 한다(Oh et al., 2014; 2020a; Lee et al., 2015). 표준 생태독성학적 연구는 주로 수생 환경 생물에 대한 영향 평가와 수생 환경에 대한 잠재적 위험성 평가를 포함하여 진행한다(Yeom and Lee, 2006). 환경생물독성 평가시에 여러 종류의 수서생물종들이 이용되는데 무척추동물로는 물벼룩, 옆새우, 가재, 완미윤충류, 어류로는 잉어, 미꾸리, 무지개송어, 자브라피쉬 등이 일반적으로 평가에 이용되고 있다(Versteeg et al., 1997). 환경 생물 독성시험 중 수생 환경 생물에 대한 시험을 진행하기 위한 시험 생물종을 선택할 때에는 실험 방법론과 생태학적 문제뿐만 아니라 생물종의 공급 및 분석 비용과 그에 따른 적합성이 고려되어야 한다(Oh et al., 2014). 본 시험에서는 환경생물 독성 시험 기준과 방법이 명시된 농촌진흥청 고시 제 2010-29호에 언급된 환경생태독성 시험 생물로서 가장 많이 사용되는 생물검정 재료중 하나인 물벼룩(Daphnia magna)을 대상으로 제초제저항성 국화에 대한 영향을 분석하였다.
본 연구에서는 모품종인 Peace copper에 제초제저항성 유전자인 phosphinothricin acetyltransferase (PAT)가 도입된 GM국화(Suh et al., 2020)를 이용하여 제초제저항성 유전자의 도입 및 발현 여부를 확인하고, 모품종인 Peace copper와 비교하여 GM국화가 물벼룩에 미치는 영향을 분석하였다. 이를 통해 제초제저항성 국화의 환경생물종에 대한 영향성을 조사함으로써 GM국화에 대한 안전성 평가 자료 생산용 급성 독성 영향 분석을 수행하였다.
Materials and Methods
시료 제조
이 실험에 사용한 GM국화는 모품종인 Peace copper에 ammonium glufosinate에 대한 저항성 유전자인 PAT가 Agrobacterium 형질전환법을 통해 도입된 제초제저항성 국화이다(Suh et al., 2020).
국립농업과학원 LMO (living modified organisms) 격리 포장(Jeonju, Korea, RDA-가AB-2013-041)에서 2022년 11월 7일에 재배한 모품종인 Peace copper와 제초제저항성 국화의 개화기 이후 잎, 줄기와 꽃을 채취하였다. 이후 실험실용 동결건조기(FD8518, IlsinBioBase, Korea)를 이용하여 시료를 완전히 건조한 후, Planetary Ball Mills (PM100, Retsch, Germany)를 이용하여 5분간 350 rpm의 조건으로 분말화하였다. 물벼룩의 급성독성 분석용 시료로 사용하기 위해 분말화된 시료는 250 µm 표준망체(Chunggye sang gong sa, Korea)로 선별 후, 시험 용수에 현탁하여 사용하였다.
게놈 DNA 추출 및 polymerase chain reaction (PCR) 검정
모품종인 Peace copper와 제초제저항성 국화의 시료는 액체질소를 사용하여 처리한 후 막자사발을 이용하여 분말화 작업을 하였다. Genomic DNA purification kit (Promega, USA)를 사용하여 각각의 분말화된 시료 100 mg에서 모품종인 Peace copper와 제초제저항성 국화의 genomic DNA를 추출하였다. 마이크로플레이트리더(Bio-Tek, USA)를 사용하여 추출된 국화의 genomic DNA를 정량 분석 하였다. 제초제저항성 국화에 도입된 T-DNA의 유전정보를 기반하여 PAT 유전자 검정을 위한 프라이머를 제작하였다(Table 1). PCR 분석을 위해 모품종인 Peace copper와 제초제저항성 국화의 genomic DNA, 프라이머 및 2X Hot Taq PCR master mix (Cellsafe, Korea)를 첨가한 후 PCR 검정을 진행하였다. 이 검정은 C100TM thermal cycler (Bio-Rad, USA)를 이용하여 진행하였고 PCR 반응은 94℃에서 5분, 94℃에서 30초, 58℃에서 30초, 72℃에서 30초의 조건으로 30회 반복하여 증폭한 후, 72℃에서 5분의 조건으로 진행하였다. PCR 산물은 1% 아가로스겔을 이용하여 전기영동 진행 및 분석하였다.
Table 1.
Primers list and sequence used for PCR (polymerase chain reaction) analysis.
| Gene | Primer | Primer sequences | Product size (bp) |
| PAT | Forward | 5′-CACTACATCGAGACAAGCAC-3′ | 450 |
| Reverse | 5′-TGAAGTCCAGCTGCCAGAAA-3′ |
제초제저항성 국화의 목적 단백질 발현 분석
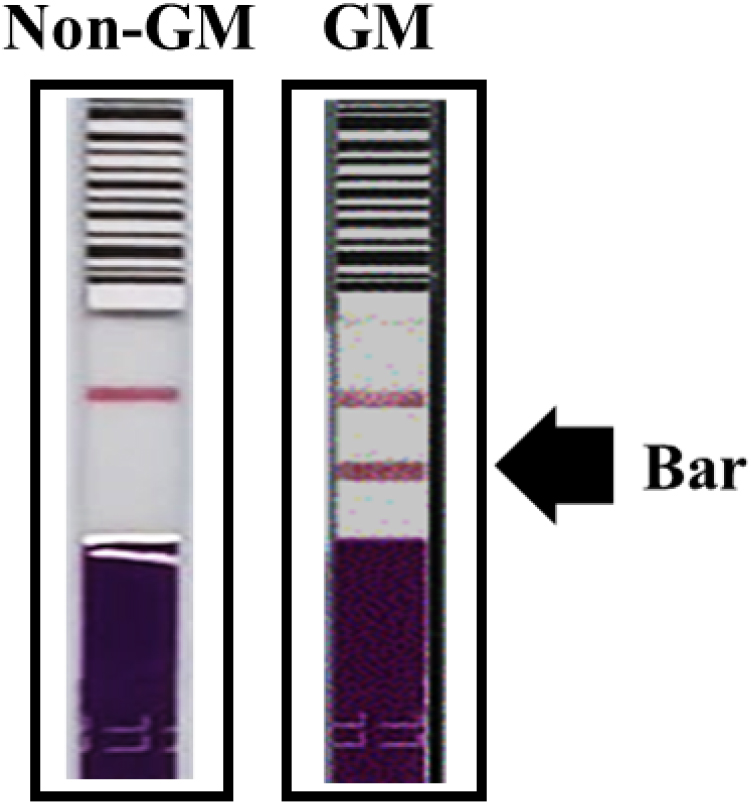
PAT 단백질 발현 검정 및 분석을 위하여 모품종인 Peace copper와 제초제저항성 국화 각각의 식물체에서 신선한 잎을 채취하여 단백질 발현 분석을 위한 시료로 활용하였다. 제조사의 매뉴얼에 따라, 채취한 식물 잎 시료를 2 mL 튜브에 증류수와 섞은 후, Biomasher II (LMS Co., Ltd., Japan)를 이용하여 단백질을 추출하였다. 단백질 발현 검정은 SeedChek™ LL PAT lateral flow test kit (Romer Labs, Austria)를 이용하여 수행하였다. 검정선(test line)과 대조선(control line)의 발현 여부를 시각적으로 확인하여 PAT 단백질의 존재를 판별하였다. 검정선이 명확하게 발현된 경우, PAT 단백질이 시료 내에 존재하는 것으로 간주하였다.
물벼룩(Daphnia magna) 배양 조건
급성독성분석용 생물종인 물벼룩은 수온 20 ± 2℃, 광조건은 500 - 1,000 Lux에서 16시간, 암조건에서 8시간의 환경에서 사육하였다. 물벼룩의 먹이는 Chlorella vulgaris (ATCC, USA)로 오전에 1회 1 × 106 cells·mL-1의 농도로 100 µL씩 공급하였다. 배양액은 adam 배지로 synthetic sea salt (Instant Ocean® Sea Salt, USA), calcium chloride dehydrate (CaCl2·2H2O, ≥99%, Duksan Pure Chemicals, Korea), sodium hydrogen carbonate (NaHCO3, ≥99%, Junsei Chemical Co., Ltd., Japan), selenium (Ⅸ) oxide (SeO2, ≥99.5%, Samchun Pure Chemical Co., Ltd., Korea)이 포함된 용액이다. 배양액인 adam 배지는 증류수 10 L에 CaCl2·2H2O, NaHCO3, SeO2 용액을 각각 23 mL, 22 mL, 1 mL 첨가하여 조제하였으며, 이때 최종 농도는 CaCl2·2H2O 0.270 g·L-1, NaHCO3 0.055 g·L-1, SeO2 0.00014 g·L-1가 되도록 하였다. 배양액은 pH 7.6 - 8.0로 맞추어 진행하였고, 경도와 알칼리도는 각각 160 - 180 mg CaCO3 L-1, 110 - 120 mg CaCO3 L-1로 유지하였다. 또한 용존산소는 3.0 mg·L-1이상 유지하여 진행하였다. 이 조건들로 만들어진 배양액은 사용하기 전 24시간 이상 폭기시켜 이용하였다. 배양액 수질 경도는 한국표준협회 KSI 3206 (KSA, 2001)의 공업용수의 시험 방법에 따라 진행하였고 알칼리도는 표준 방법(APHA et al., 2005)에 따른 염산적정법으로 측정하였다. 그 결과, 시험에 영향을 줄 수 있는 어떠한 요인도 발견되지 않았음을 확인하였다.
물벼룩에 대한 시료 처리 조건
국화에 대한 물벼룩 급성독성시험을 진행하기 전에 non-GM국화인 Peace copper와 제초제저항성 국화의 각 시료에 대한 48시간동안 예비 실험을 진행하였다. 예비 실험은 0, 500, 1,000, 2,000, 5,000, 10,000 및 20,000 mg·L-1의 농도로 진행하였다. 48시간 동안 non-GM국화와 제초제저항성 국화에 대한 유효농도 분석을 진행한 결과, EC50 (effective concentration 50)값이 211.4 - 532.5 mg·L-1범위 내에 포함된다는 결과가 나왔다. 이를 근거로, 물벼룩에 대해 0, 50, 100, 200, 500, 1,000 및 2,000 mg·L-1의 7가지의 농도로 시료를 처리하였다. 시험용액을 만들기 위해 각각 100 mL의 시험용수에 시료(0.005, 0.010, 0.020, 0.050, 0.100 및 0.200 g)를 반복 처리하여 사용하였다. 시험용수인 adam배지를 음성대조구로 이용하였다. Adam 배지, non-GM국화와 제초제저항성 국화 모두 135 mL 용량의 원통형 유리수조(65 mm Height × 57 mm ϕ)에 7가지의 농도로 100 mL씩 처리하였다. 또한 각 수조에 생후 24시간 이내의 어린 물벼룩을 대상으로 농도 당 각 10마리씩 넣어 3반복 실시하였다. 그리고 수온은 사육조건과 같이 19 - 21℃를 유지하였다.
물벼룩 급성 독성 시험 조사 및 평가 항목
각 처리구에 대하여 24시간 및 48시간 후 일반중독증상, 특이증상 및 유영저해 개체수 등이 물벼룩에 대한 급성 독성 평가를 위한 조사 항목에 포함된다. 일반 중독된 물벼룩은 운동성 저하, 반응성 둔화, 무기력한 증상 등으로 판단하였다(OECD, 2004). 특이증상을 보이는 물벼룩은 체색 변화, 형태 이상 등 특정 독성 물질에 의한 반응 등으로 확인하였다(Friberg-Jensen et al., 2010). 유영저해 물벼룩은 시험용기를 약하게 흔들고 15초 후에 촉각과 후복부 등은 움직이지만 유영은 하지 못하는 것으로 판단하였다. 물벼룩에 대한 급성독성시험기간 중 시료 처리직후, 24시간 경과후와 종료 시의 각 처리구에 대하여 pH 및 dissolved oxygen (DO)을 측정하였고 수온은 24시간 간격으로 측정 및 기입하였다. Mettler Toledo 사의 SevenGo Duo pH/lon/DO meter SG 98 (Mettler Toledo, Swithzerland)을 이용하여 시험용수의 pH, DO값과 수온을 분석하였다. 중독증상이 없고 또한 유영저해가 발생하지 않는 최고 시험농도를 무영향농도(no observed effect concentration, NOEC)로 정의하였다. 그리고 반수영향농도(EC50 및 95% 신뢰한계)는 미국 환경보호청의 시험지침서(USEPA, 1985)에 따라 Probit 분석법을 통해 산출하였다. 시험물질 처리 후 24시간 및 48시간에서 유효성분의 반수영향농도 각 농도에서의 반응률을 백분율로 환산한 뒤, 이를 probit 값으로 변환하여 산출하였다.
Results and Discussion
제초제저항성 국화의 유전자 도입 유전자 검정
제초제저항성 국화의 시료에 제초제저항성 유전자인 PAT가 도입되어 있는 지를 검정하기 위해 non-GM국화와 제초제저항성 국화의 genomic DNA로 PCR 분석을 실시하였다. PCR 분석 결과 non-GM국화의 genomic DNA에서는 PAT 유전자가 검출되지 않았고 제초제저항성 국화의 genomic DNA에서는 PAT 유전자가 검출되었다. PCR 분석을 통해 물벼룩 급성 독성 평가에 사용된 제초제저항성 국화에 PAT 유전자가 정상적으로 도입되었음을 확인하였다(Fig. 1).
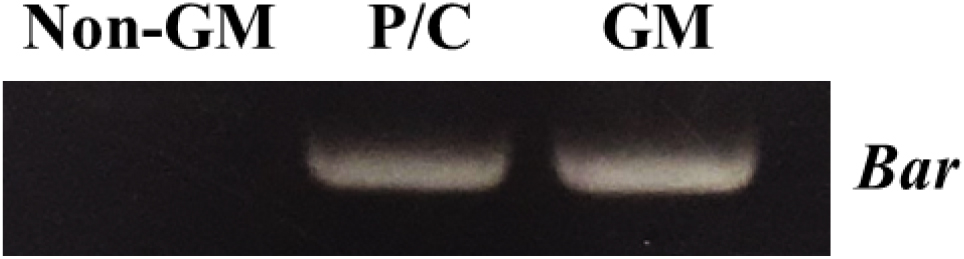
Fig. 1.
Confirmation of the bar genes on the genetically modified (GM) chrysanthemum. Non-GM, Chrysanthemum morifolium Ramat.; P/C, plasmid DNA of pCB302 vector with bar gene (Jang et al., 2024) for positive control; GM, herbicide-resistant transgenic chrysanthemum; Bar, herbicide-resistant gene.
물벼룩 급성 독성 평가에 사용된 제초제저항성 국화에 제초제 저항성 형질의 도입 여부를 확인하기 위해 non-GM국화와 제초제저항성 국화의 시료들을 사용하여 PAT 단백질의 항체를 이용한 immunostrip 분석을 수행하였다. Immunostrip 검정 결과, 제초제 저항성 형질이 도입된 시료에서는 테스트 라인(test line)과 대조 라인(control line)이 모두 발현되었으며, 이는 제초제저항성 국화 내 PAT 단백질이 정상 발현되고 있음을 의미한다. 반면, 모본 품종에서는 테스트 라인이 나타나지 않아 단백질이 비발현 상태임을 확인하였다. 이를 통해 PAT 단백질은 non-GM국화에서 검출되지 않았고 제초제저항성 국화에서는 발현함이 확인되었다(Fig. 2).
시료처리용 시험용수의 수질변화 검정
본 시험에 사용된 시험 용수에 대한 수질검사는 제초제저항성 국화와 non-GM국화의 모든 처리구 시험 용수의 온도와 pH, 용존산소량 등을 하루 1회씩 측정하고 기입하여 시험 용수의 수질 변화를 확인하였다. 시험기간 중 시험용수의 수온은 제초제저항성 국화 처리구에서는 평균 20.8 ± 1.0℃ (19.2 - 21.6℃)이었고, non-GM국화 처리구에서는 평균 20.9 ± 1.0℃ (19.3 - 22.0℃)로 측정되었다. 이는 농촌진흥청고시 제 2010-29호 환경생물 독성 시험기준에 제시된 적정 실험온도인 18 - 22℃의 범위에 포함되는 조건으로, 실험온도의 변화가 독성 평가의 영향 요소로는 작용하지 않음을 확인하였다(Table 2). 시험용수의 pH는 0시간 처리조건에서 제초제저항성 국화와 non-GM국화의 농도별 처리구에서 각각 7.50 (6.93 - 8.01) 및 7.55 (7.02 - 8.09)으로 나타났다. 그리고 48시간 경과 후에는 각각 7.40 (6.96 - 7.93) 및 7.25 (5.70 - 7.90)로 측정되었다(Table 3). 제초제저항성 국화와 non-GM국화의 처리농도에 따라 pH가 낮아지는 경향을 보였는데, 이는 물벼룩의 호흡과 같은 생리 작용과 유기물 분해 작용 등에 영향을 의한 것으로 판단되며(Hilbeck et al., 2017), 도입유전자에 따른 통계적 유의차가 없음을 확인하였다. 예비시험의 수질검사 측정결과를 바탕으로 시험용수의 DO값이 포화용존산소량의 60% 이하로 떨어지는 것을 방지하기 위하여 24시간 간격으로 시험용수에 30분간 산소를 공급하였다. 0시간(시험용수에 시료를 현탁한 시점)에서 시험용수의 DO는 제초제저항성 국화와 non-GM국화에 대하여 각각 7.96 mg·L-1 (7.47 - 8.48 mg·L-1) 및 7.82 mg·L-1 (7.08 - 8.29 mg·L-1)이었으며, 처리 48시간 후에는 각각 7.67 mg·L-1 (6.14 - 8.36 mg·L-1) 및 7.62 mg·L-1 (6.01 - 8.39 mg·L-1)로 측정되었다. 시험기간 중 처리농도별 제초제저항성 국화와 non-GM국화간의 DO는 유의적인 차이가 없었다. 처리시간에 따른 DO의 감소는 제초제저항성 국화와 non-GM국화의 경우 유기물인 시료를 처리하였으므로 DO수치가 급격히 감소되는 경향을 보인 반면, 음성대조구(0 mg·L-1)는 0시간 및 48시간에 각각 8.06 mg·L-1 (7.76 - 8.48 mg·L-1) 및 7.96 mg·L-1 (7.08 - 8.36 mg·L-1)로써 소폭 감소하는 경향을 보였다(Table 4). 위 결과들을 종합해 보면, 본 실험에 이용된 시험 용수의 수온 및 pH와 용존산소량 등은 물벼룩 급성독성시험에 유의한 영향을 미치지 않는 것으로 판단된다.
Table 2.
Changes of water temperature (℃) during cumulative mortality tests of Daphnia magna in Non-GM and GM chrysanthemums.
Table 3.
Changes of pH during cumulative mortality tests of Daphnia magna in Non-GM and GM chrysanthemums.
Table 4.
Changes of dissolved oxygen (DO) during cumulative mortality tests of Daphnia magna in Non-GM and GM chrysanthemums.
제초제저항성 국화와 non-GM국화의 처리 농도별 물벼룩의 유영저해 변화
대표적인 수서환경생물종인 물벼룩은 무기독성물질과 유기독성물질 모두에 예민하게 반응하기 때문에 급성 독성 시험시 24시간 및 48시간 후에 유영저해에 대한 평가를 수행한다(Oh et al., 2014). 이 물벼룩 급성독성시험을 위해 제초제저항성 국화와 non-GM국화를 지수식으로 농도당 처리된 시료에 물벼룩 10마리를 노출시켜 48시간 동안 일반중독증상 및 생사수 관찰을 조사하였고 총 3반복 실시하였다(Oh et al., 2020b).
제초제저항성 국화의 시료 처리결과 물벼룩 생육은 24시간과 48시간 후에 50 및 100 mg·L-1 농도 조건에서 유영저해를 보이지 않았다. 그러나 200 mg·L-1 및 500 mg·L-1 처리농도에서는 각각 24시간 후에는 10% 및 33.3%, 48시간 후에는 30.0% 및 63.3%의 유영저해를 보였고, 1,000 mg·L-1 및 2,000 mg·L-1 처리농도에서는 24시간 후에는 73.3% 및 86.7%, 48시간 후에는 모두 100% 유영저해를 보였다. Non-GM국화 시료처리구에서는 24시간 및 48시간 후 50 mg·L-1 및 100 mg·L-1 농도에서 유영저해를 보이지 않았다. 그러나 200 mg·L-1 및 500 mg·L-1 처리농도에서는 각각 24시간 후에는 10.0% 및 33.3%, 48시간 후에는 33.3% 및 63.3%의 유영저해를 보였고, 1,000 mg·L-1 및 2,000 mg·L-1 처리농도에서는 24시간 후에는 73.3% 및 86.7%, 48시간 후에는 모두 100% 유영저해를 보여, 제초제저항성 국화 처리가 non-GM국화에 비하여 유영저해에 심화시키는데 영향을 미치지 않았다(Table 5). 음성대조군(0 mg·L-1)에서는 처리기간 중 일반중독증상과 특이증상이 관찰되지 않았으며, 제초제저항성 국화와 non-GM국화 처리구에서는 각각 100 mg·L-1 및 50 mg·L-1 이상의 조건에서 일반중독 증상을 보이는 개체가 관찰되었다. 그러나 제초제저항성 국화와 non-GM국화 처리구 간의 통계적 유의차는 없었으며 이를 바탕으로 제초제저항성 국화가 일반중독 증상에 영향을 미치지 않은 것으로 사료된다(Table 5).
Table 5.
Cumulative immobility of Daphnia magna in Non-GM and GM chrysanthemums.
제초제저항성 국화와 non-GM국화의 급이에 의한 물벼룩에 대한 급성독성
제초제저항성 국화와 non-GM국화의 급이에 의한 물벼룩에 대한 급성독성시험을 실시하였고 그 결과 48시간-EC50은 non-GM국화는 333.6 mg·L-1 (95% 신뢰한계: 211.4 - 526.2 mg·L-1), 제초제저항성 국화는 348.5 mg·L-1 (95% 신뢰한계: 228.1 - 532.5 mg·L-1)로 제초제저항성 국화가 보다 높은 급성독성을 보였다. 하지만 제초제저항성 국화가 95% 신뢰한계 구간 내의 차이만 보여 통계적으로 유의성은 없는 것으로 나타나 급성 독성에는 영향을 미치지 않은 것으로 사료된다. 무영향 농도(NOEC)는 두 품종 모두 100 mg·L-1으로 확인되었고(Table 6), 이에 따라 제초제저항성 국화와 non-GM국화가 물벼룩에 미치는 독성에 차이가 없음을 알 수 있다. 따라서 PAT 유전자가 형질전환된 제초제저항성 국화 및 non-GM국화가 물벼룩에 미치는 영향 평가를 진행하였고 그 결과, 제초제저항성 국화와 non-GM국화의 EC50값이 348.5 mg·L-1, 333.6 mg·L-1으로 비슷한 양상의 실험결과를 보였고 무영향 농도(NOEC) 또한 100 mg·L-1으로 같은 결과를 나타났다. 이는 물벼룩에 대한 PAT 단백질 노출이 물벼룩에 부정적인 영향을 미치지 않는 것으로 사료된다.
Table 6.
EC50 values of Daphnia magna after 48 hours in Non-GM and GM chrysanthemums.
| Test item | EC50 (mg·L-1) | NOEC (mg·L-1) |
| Control | - | - |
| Non-GM |
333.6 (211.4 - 526.2)z | 100 |
| GM |
348.5 (228.1 - 532.5) | 100 |
제초제저항성 국화에 대한 독성 위해성 평가는 수서환경생물종인 잉어에 대해 실시된 바 있으며, 잉어에 대한 급성독성시험 결과 non-GM국화와 유의적 차이가 없음이 확인되었다(Jang et al., 2025). 이처럼 어류를 이용한 독성 위해성 평가를 위해서는 수서환경생물종인 잉어나 물벼룩 이외에도 미꾸리, 제브라피쉬 등 다양한 비표적 생물종에 대한 독성 영향 분석이 이뤄지고 있다. 그러나 현재까지 수행된 환경위해성평가는 주로 콩이나 벼와 같은 식용작물에서 이뤄지고 있는 실정이다. 본 연구는 국화를 포함한 GM화훼 작물에 대한 독성 위해성 연구 기준을 구축하기 위한 기초자료로써 활용가치가 있을 것으로 판단되며 추후 GM국화를 대상으로 추가적인 농업환경생물종에 대한 영향 평가가 수행되어야 할 것이다.
Conclusion
본 연구는 제초제저항성 유전자를 Peace copper에 형질전환시킨 제초제저항성 국화의 환경위해성 평가에 대한 기초 자료 및 안전성 평가 가이드라인을 개발하고자 제초제저항성 국화에 도입된 PAT 유전자의 발현 분석과 검증 및 수서 생물종인 물벼룩에 미치는 영향을 비형질전환 국화인 Peace copper와 비교 분석을 수행하였다. 제초제저항성 국화에 도입된 PAT 유전자의 PCR 분석 결과, 제초제저항성 국화에서만 특이적인 밴드가 검출되었다. 제초제저항성 국화와 non-GM국화의 물벼룩에 대한 급성독성시험을 실시한 결과, non-GM국화의 48시간-EC50는 333.6 mg·L-1 (95% 신뢰한계: 211.4 - 526.2 mg·L-1), 무영향농도(NOEC)는 100 mg·L-1였고, 제초제저항성 국화의 48시간-EC50는 348.5 mg·L-1 (95% 신뢰한계: 228.1 - 532.5 mg·L-1)였으며, 무영향농도는 100 mg·L-1이었다. 처리기간 중 물벼룩에 대한 급성독성에 제초제저항성 국화와 non-GM국화가 영향을 미치지 않았다. 따라서 제초제저항성 국화 급이가 물벼룩에 특별한 독성을 보이지 않는 것으로 판단된다.