Introduction
Materials and Methods
시험농약
시약 및 기구
포장정보
시험물질 처리
시료 수확
시료의 추출, 정제
토양성분
검량선 작성
저장안정성 시험
통계분석
Results and Discussion
분석결과
시험기간 중 작물 생육
저장안정성 시험 결과
시료 분석
토양분석
Conclusion
Introduction
농약은 현대 농업에 있어 필수적인 농업자재로서 다양한 화학물질로 구성되어 있으며 농산물의 재배에 있어 병, 해충, 잡초에 의한 작물 손실방지, 생산량 증대, 그리고 품질을 향상시키는 등 중요한 역할을 한다. 이러한 장점에도 불구하고 독성과 잔류안전성 등으로 인해 농약의 남용은 인체, 작물 및 환경 등에 악영향을 야기하고 있는 것으로 보고되었다(Lee et al., 2015).
토양에 살포된 농약은 토양 입자에 흡착되거나 미생물 및 화학적 작용에 의해 분해되나, 일부 화합물과 그 산화대사물은 토양 내에서 비교적 장기간 잔류할 수 있다. 이러한 잔류성 물질은 흙 입자에 부착되거나 용탈·이동하여 후작물의 뿌리를 통해 흡수되어 식물체 내로 전이되며, 결과적으로 의도하지 않은 농산물 오염 및 식품 안전성 문제가 발생할 수 있다(FAO and WHO, 2006; Namiki, 2022). 특히 terbufos의 산화대사물인 sulfoxide 및 sulfone은 모화합물보다 토양에서 더 긴 반감기(50% disappearance time, DT50)와 더 큰 이동성을 보여 토양 내 축적 및 작물로의 전이 가능성이 보고되어 있다(EPA, 2015; Sarker et al., 2023). 따라서 전작물-후작물 연계에서 토양의 잔류 및 작물 전이 특성을 규명하는 연구가 요구된다.
Terbufos는 살충 효과가 뛰어나고 경제성이 높아 다양한 작물에 광범위하게 사용되는 유기인계 농약이다. Terbufos는 작물과 토양 내에서 가수분해 및 산화 과정을 거쳐 여러 대사물이 생성되며, 이들 산화 대사물은 독성학적 우려로 인해 잔류물 정의에 포함된다. 또한 환경에서의 안정성이 높아 장기간 잔류할 가능성이 있는 것으로 보고되었다(Lee et al., 2025).
특히, 국내 농산물 안전성 조사에서 terbufos는 부적합 검출 빈도가 높은 농약 성분 중 하나로 보고되어, 후작물로의 흡수 가능성과 식품 안전성 문제를 야기할 수 있는 대표적 사례로 지목되고 있다(MAFRA and NAQS, 2023). 이러한 점은 terbufos를 연구 대상으로 선정한 타당성을 뒷받침하며, 전작물-후작물 연계에서의 잔류 및 전이 특성을 규명하는 연구가 시급히 필요하다.
Terbufos는 토양과 식물 내에서 대사 과정을 거쳐 terbufos oxon, terbufos oxon sulfone, terbufos oxon sulfoxide, terbufos sulfone, terbufos sulfoxide와 같은 최종 산화 대사산물로 전환되며, 이들 대사산물은 원물질인 terbufos보다 더 강한 독성을 나타내는 것으로 보고되고 있다. 최근 연구들에서는 terbufos의 산화대사물인 sulfoxide 및 sulfone이 모화합물보다 토양에서 상대적으로 안정하고 더 긴 반감기를 보이며 작물로의 전이 가능성이 높다고 보고되고 있다(e.g., Choung et al., 2011; Elsner and Imfeld, 2016). 초기의 연구(Hong et al., 1986)는 이러한 현상을 최초로 보고한 보조적 근거로 참고하였다. 본 연구에서는 tebufos의 여러 대사체 중에서도 환경에서 안정성과 독성 우려가 가장 큰 sulfoxide 및 sulfone 대사체를 중심으로 잔류 특성을 규명하고자 하였다.
따라서 본 연구는 terbufos의 토양 내 거동과 작물 전이 특성을 규명하는 것을 목표로 하였다. 구체적으로, terbufos가 처리된 토양에서 전작물(대파)을 재배하여 terbufos 및 그 산화 대사체의 흡수·소실 특성을 확인하고, 동일한 토양에서 추가 농약 살포 없이 후작물(머위)을 재배하여 토양 잔류물이 후작물로 전이되는 정도를 평가하고자 하였다. 이를 통해 주요 산화 대사체(sulfoxide, sulfone)의 잔류 특성을 명확히 하고, 향후 안전성 관리 기준 마련에 필요한 기초자료를 제공하고자 하였다.
Materials and Methods
시험농약
본 연구에서 사용된 농약은 경농㈜에서 제조한 말뚝 입제(terbufos 3%)를 구입하여 실험에 활용하였다. 또한, 각 농약의 표준품은 AccuStandard (USA)에서 구입한 1,000 mg·L-1 농도의 액상 표준품을 사용하였으며, 시험성분의 특성은 Tables 1과 2와 같다.
Table 1.
Physicochemical properties of terbufos.
Table 2.
IUPAC names, molecula weight, and molecular formula of terbufos and its metabolites.
시약 및 기구
연구에 사용된 모든 시약은 잔류분석에 적합한 HPLC 등급의 시약을 사용하였고, 시험에 사용된 주요 시약 및 시험기구는 Tables 3과 4와 같다.
Table 3.
Reagents used for terbufos residual analysis.
Table 4.
Apparatus used for terbufos residual analysis.
포장정보
본 연구는 전작물(대파, 품종: 흑금장파)과 후작물(머위, 품종: 참머위)에 대한 terbufos 잔류행동을 평가하기 위해 다음과 같이 시험포장을 구성하였다.
시험포장은 강원도 영월군 영월읍 동강로 716에 위치한 비닐하우스 내, 최근 terbufos를 포함한 농약 살포 이력이 없는 구역을 선정하였고 토양시료를 측정하여 확인하였다. 총 7구역(3 m × 3 m)으로 구성하였으며, 무처리구 1구역, 권장량 처리구(1×) 3구역, 5배 처리구(5×) 3구역을 배치하였다. 처리구 간 교차오염을 방지하기 위해 각 구획 사이에 1 m 이상의 완충 구간을 두었다.
파종(정식)은 전·후작물 모두 재식밀도 10 cm × 10 cm가 되도록 시행하였다. 전작물인 대파는 정식 직후(0일차)에 terbufos를 처리한 후 30일간 재배하였으며, 재배 30일차에 뿌리·줄기·잎 부위별로 시료를 채취하였다. 이후 10일간의 휴경기를 거치고, 후작물인 머위를 동일 포장에 정식하여 30일간 재배하였다. 머위 재배 기간 동안의 평균 기온은 17.3 - 25.7℃, 평균 상대습도는 74.1 - 88.3%로 기록되었으며, 농가의 관행적인 재배 방법을 따랐다. 후작물 채취 시에는 지상부 전체를 대상으로 시료를 수집하였다.
시험물질 처리
처리량은 농촌진흥청 농약안전정보시스템(RDA, 2024)에 제시된 대파 정식 재배 시 안전사용기준인 6 kg·10a-1를 기준으로 하였으며, 이를 1배 처리구로 설정하고, 비교를 위하여 5배 처리구(30 kg·10a-1)를 추가하였다. 머위는 본 약제가 등록되지 않은 작물이므로, 후작물로의 전이 가능성을 평가하기 위한 시험 작물로만 사용하였다.
시험구 면적은 3 m × 3 m (9 m2)로, 1배 처리구의 제제량은 54 g이며, 유효성분 3% 함량을 고려한 실제 투입량은 약 1.62 g이다. 5배 처리구는 제제량 270 g, 유효성분 투입량은 약 8.10 g으로 산정되었다.
약제는 실험자가 손에 고무장갑을 착용한 상태에서 직접 9 m2 시험구에 산정된 제제량을 고르게 살포하였으며, 균일한 분포에 주의하였다. 살포 후에는 수작업 농기구를 이용하여 토양 0 - 10 cm 깊이까지 균일하게 경운하고 혼화하였다.
시료 수확
토양에 terbufos 입제를 목표 농도로 처리한 후, 전작물인 대파를 재배하였다. 대파는 처리 후 30일차에 뿌리, 줄기, 잎 부위별 시료를 채취하였으며, 동시에 토양 시료도 10일 간격으로 수집하여 농약 잔류 및 반감기를 분석하였다. 전작물 수확 후 10일간의 휴경기를 거쳐 동일 시험구에서 후작물인 머위를 0일간 재배하였다. 머위의 경우, 농약 살포 후 40, 50, 60, 70일의 10일 간격으로 지상부 전체를 무작위로 채취하여 잔류 농약 분석에 사용하였다. 약제 살포일을 0일로 하여 0일차 시료는 농약이 완전히 건조된 후 채취하였으며, 무처리 시료는 동일한 날 처리구 시료 채취 직전에 수집하였다. 시험구당 최소 500 g 이상의 머위 시료를 무작위로 채취한 후, 지퍼백에 담아 실험실로 운반하였다. 토양 시료의 경우 표층(0 - 10 cm) 토양을 시료당 1 kg 이상 채취한 뒤, 2 mm 체로 균질화하고 폴리에틸렌 백에 밀봉하여 냉동보관 한 후 분석 시료로 사용하였다. 운반 시, 시료의 온도 유지를 위해 아이스팩을 포함한 아이스박스를 사용하였다. 전작물 파는 파종 후 30일차에 일시 수확하여 지상부와 지하부의 토양입자를 제거하고 균질화 하여 -20 ± 2℃의 냉장고에 보관하였다. 후작물 머위는 전작물 수확 후 10일 뒤 연작하였다. 후작물 머위는 토양입자를 제거하고 믹서기로 분쇄하여 분석을 진행하였으며, 분석 후에는 -20 ± 2℃의 냉동고에 보관하였다.
시료의 추출, 정제
토양, 파, 머위의 잔류농약 분석법은 국립농산물품질관리원 공고 제2024-44호의 농산물 잔류농약 분석방법을 참고하여 분석하였다.
머위와 토양 시료는 각각 10 g과 5 g을 50 mL 용량의 원심분리관에 칭량한 후 물 10 mL을 넣고 30분간 방치하였다. 방치 후 acetonitrile 10 mL를 첨가하여 2분간 진탕한 후 QuEChERS Extraction kit (EN method; Chromatific, Germany; 무수황산마그네슘[MgSO4] 4 g, 염화나트륨[NaCl] 1 g, 구연산이나트륨·1.5수화물[Na2H(C6H5O7)·1.5H2O] 0.5 g, 구연산삼나트륨·2수화물[Na3C6H5O7·2H2O] 1 g)를 첨가하고 1분간 다시 진탕하였다. 원심분리(4,000 rpm, 5분) 후 상등액 1 mL를 dSPE (dispersive solid-phase extraction; primary secondary amine [PSA] 25 mg, MgSO4 150 mg)에 첨가하여 3,500 rpm에서 1분간 진탕한 후, 4,000 rpm에서 5분간 원심분리하였다. 최종 상등액 1 mL를 0.2 µm 멤브레인 필터로 여과한 후, 고성능액체크로마토그래피 탠덤 질량 분석기(high-performance liquid chromatography-tandem mass spectrometry, HPLC-MS/MS) 분석을 위해 acetonitrile 300 µL 및 0.1% 포름산과 5 mM 아세트산암모늄 함유 water 600 µL로 희석하였다.
토양성분
시험 토양의 물리화학적 특성은 Table 5에 정리하였다. 모래 40.7%, 미사 38.0%, 점토 11.3%로 구성되어 토성은 양토(loam)를 나타내었고 유기물 함량이 30 g·kg-1, 전기전도도가 0.69 dS·m-1, pH가 6.4, 유효인산 400 mg·kg-1, 치환성 칼륨 0.3 cmol+·kg-1, 치환성 칼슘 5.3 cmol+·kg-1, 치환성 마그네슘 2.2 cmol+·kg-1으로 본 시험작물인 대파 및 머위를 재배하는데 적합한 토양이었다.
Table 5.
Physicochemical properties of the Welsh onion and butterbur-cultivated soils.
| Soil texture |
pH (1 : 5) | Exchangeable cations (cmolc·kg-1) |
OM (g·kg-1) |
EC (dS·m-1) | Particle distribution (%) | ||||
| K | Ca | Mg | Sand | Silt | Clay | ||||
| Loam | 6.4 | 0.3 | 5.3 | 2.2 | 30 | 0.69 | 40.7 | 38.0 | 11.3 |
검량선 작성
Terbufos 표준품 1,000 mg·L-1을 stock solution으로 사용하였다. 이 stock solution을 acetonitrile으로 희석하여 0.005, 0.010, 0.020, 0.050, 0.100, 0.200, 0.500 mg·L-1으로 만든 후 standard : 무처리 추출액 : acetonitrile = 1 : 2 : 7 비율로 섞어 0.0005, 0.0010, 0.0020, 0.0050, 0.0100, 0.0200, 0.0500 mg·L-1 수준의 matrix matched standard를 제조하였다. 이를 LC-MS/MS에 2 µL 주입하여 나타난 chromatogram상의 peak 면적을 기준으로 검량선을 작성하였다. 분석에 사용된 LC-MS/MS 기기조건과 multiple reaction monitoring (MRM) 조건은 Tables 6과 7과 같다.
Table 6.
LC-MS/MS conditions for analysis of terbufos.
Table 7.
LC-MS/MS conditions for the residual analysis of terbufos metabolites.
저장안정성 시험
저장 안정성 시험은 시료 보관 중 terbufos 및 그 산화대사체의 안정성을 검증하기 위하여 수행하였다. 이를 위해 처리구에서 채취한 시료를 -20℃에서 150일 저장한 후 분석하여, 저장 기간에 따른 성분의 분해 여부를 확인하였다.
통계분석
모든 결과는 평균 ± 표준편차로 제시하였다. 처리 수준(1×, 5×) 및 부위별(뿌리·줄기·잎) 잔류량 차이는 분산분석(ANOVA)을 통해 검정하였으며, 유의성이 나타날 경우 Tukey의 다중비교검정(Tukey’s HSD test)을 수행하였다(p < 0.05). 또한 특정 두 처리구 간 차이는 Student’s t-test로 비교하였다. 모든 통계적 유의성은 p < 0.05 수준에서 판정하였다.
Results and Discussion
분석결과
회수율 시험 결과
본 연구에서 수행한 회수율 시험 결과, terbufos의 평균 회수율은 머위에서 90.42 - 101.85%, 토양에서 91.22 - 99.59%로 나타났으며, 각 처리 농도(limit of quantification [LOQ] 0.01 mg·kg-1의 1×, 5×, 10×)에서 5반복 실험의 표준편차는 모두 10% 미만으로 확인되었다. 또한 LC-MS/MS 분석 과정에서 간섭 피크는 검출되지 않아, 분석법의 선택성이 확보되었음을 확인하였다.
국제적으로 잔류농약 분석법의 회수율은 70 - 120%, 상대표준편차(relative standard deviation, RSD)는 20% 이하를 기준으로 제시되고 있으며(EC, 2019), 국내 식약처(MFDS, 2018)의 가이드라인에서는 반복성 RSD ≤ 10%를 권장한다. 본 연구의 회수율 및 정밀도는 이러한 국제 및 국내 기준을 모두 충족하였다.
선행연구와 비교한 결과, 미국 환경보호청(EPA, 2017)의 검증 자료에서는 terbufos와 그 산화대사체(설폭사이드, 설폰)의 평균 회수율이 수계 매트릭스에서 95 - 99%, RSD 4 - 8% 범위로 보고되었으며, 이는 본 연구 결과와 유사한 수준이다. 또한 다성분 LC-MS/MS 방법을 적용한 유럽 지역 연구들에서도 식물성 매트릭스 내 잔류농약의 회수율은 주로 85 - 105% 범위에 분포하는 것으로 보고되어(Takatori et al., 2013; Yuan et al., 2022), 본 연구의 수치가 통상적인 우수 범위에 해당함을 확인할 수 있다. 반면 일부 연구에서는 정제 단계에서 그래파이트 카본 블랙(graphitized carbon black, GCB)을 사용할 경우, 평면 구조(planar structure)를 가진 농약 성분이 흡착되어 회수율이 감소할 수 있다고 보고된 바 있다(Lehotay et al., 2005). 특히 terbufos 역시 GCB에 부분적으로 흡착되어 회수율 저하를 보인다는 보고가 있으나, 본 연구에서는 간섭 피크 없이 90% 이상의 안정적인 회수율을 확보하여 추출 및 정제 조건이 적절하게 설정되었음을 확인하였다.
또한 국제식품규격위원회(Codex) 및 FAO and WHO (2006) 평가 자료에 따르면 terbufos의 검출한계(limit of detection, LOD)와 정량한계(LOQ)는 대체로 0.01 - 0.05 mg·kg-1 수준으로 보고되고 있으며(FAO and WHO, 2016), 본 연구에서 설정한 LOQ 0.01 mg·kg-1은 국제적 기준과 부합한다.
종합적으로, 본 연구의 회수율 시험 결과는 국내외 가이드라인 기준을 충족할 뿐만 아니라, 선행 연구에서 보고된 terbufos 회수율 범위와도 일치한다. 따라서 본 연구에서 적용한 LC-MS/MS 기반 분석법은 머위 및 토양 시료 중 terbufos의 잔류분석에 적합하고 신뢰할 수 있는 분석법으로 평가된다.
시험기간 중 작물 생육
전작물인 대파의 수확 시 부위별 평균 무게는 뿌리 3.19 ± 0.16 g, 줄기 64.7 ± 3.4 g, 잎 37.11 ± 0.14 g으로 나타났다. 평균 길이는 각각 뿌리 3.10 ± 0.43 cm, 줄기 25.43 ± 1.74 cm, 잎 30.91 ± 1.34 cm이었다. 후작물인 머위의 경우, 지하부 평균 무게는 1차 수확 시 0.79 g에서 최종 수확 시 2.61 g으로 증가하였으며, 지상부는 10.46 g에서 30.14 g으로 약 3배 증가하였다. 처리 수준(1배 처리구와 5배 처리구) 간에는 유의적인 차이가 없었다.
저장안정성 시험 결과
시료를 냉동 보관하는 동안 분석대상농약의 경시변화 정도를 평가하기 위하여 저장안정성시험이 수행되었다. 무처리 시료에 0.5 mg·kg-1 수준의 terbufos 표준용액을 처리하고 분석 전까지 -20℃의 냉동고에 보관한 후 시료와 함께 전처리하여 회수율을 조사하였다. 저장안정성시험 결과, 회수율은 90.1 - 99.2% 범위로서 저장기간 중 매우 안정한 것으로 평가되었다(Table 8).
Table 8.
Storage stability test result of terbufos.
시료 분석
전작물 대파 중 terbufos의 잔류량
모화합물인 terbufos의 잔류량은 뿌리에서 기준량(1배) 처리 시 LOQ (< 0.01 mg·kg-1) 미만이었고, 5배 처리구에서 0.013 ± 0.004 (0.001 - 0.018) mg·kg-1이었다. 줄기에서는 기준량(1배) 처리 시 LOQ 미만이었으며, 5배 처리 시 0.021 ± 0.005 (0.015 - 0.027) mg·kg-1이 검출되었다. 잎에서는 1배 처리 시 LOQ 미만, 5배 처리 시 0.014 ± 0.003 (0.010 - 0.018) mg·kg-1이 확인되었다.
대사체의 경우, 1배 처리구에서 뿌리는 모두 LOQ 미만이었으나, 줄기에서는 terbufos sulfoxide가 0.011 ± 0.002 (0.009 - 0.013) mg·kg-1 검출되었고, 잎에서는 terbufos sulfone 0.013 ± 0.003 (0.009 - 0.017) mg·kg-1, sulfoxide 0.011 ± 0.002 (0.009 - 0.014) mg·kg-1이 검출되었다.
5배 처리구에서 뿌리에서는 terbufos oxon 및 oxon sulfone은 LOQ 미만이었으나, oxon sulfoxide 0.013 ± 0.003 (0.010 - 0.017) mg·kg-1, sulfone 0.063 ± 0.008 (0.054 - 0.073) mg·kg-1, sulfoxide 0.052 ± 0.007 (0.044 - 0.061) mg·kg-1이 검출되어 총잔류량은 0.132 ± 0.011 (0.120 - 0.145) mg·kg-1이었다. 줄기에서는 oxon은 LOQ 미만, oxon sulfone 0.023 ± 0.004 (0.018 - 0.028) mg·kg-1, oxon sulfoxide 0.027 ± 0.005 (0.021 - 0.033) mg·kg-1, sulfone 0.082 ± 0.010 (0.070 - 0.095) mg·kg-1, sulfoxide 0.073 ± 0.009 (0.062 - 0.085) mg·kg-1이 검출되어 총잔류량은 0.213 ± 0.016 (0.197 - 0.230) mg·kg-1이었다. 잎에서는 oxon은 LOQ 미만, oxon sulfone 0.019 ± 0.003 (0.015 - 0.023) mg·kg-1, oxon sulfoxide 0.023 ± 0.004 (0.018 - 0.028) mg·kg-1, sulfone 0.072 ± 0.009 (0.061 - 0.083) mg·kg-1, sulfoxide 0.065 ± 0.008 (0.056 - 0.075) mg·kg-1이 검출되어 총잔류량은 0.181 ± 0.013 (0.168 - 0.197) mg·kg-1이었다(Table 9).
본 연구에서 확인된 바와 같이, 지상부(줄기 및 잎)에서는 sulfoxide와 sulfone이 주요 잔류형으로 나타났으며, 이는 FAO and WHO (2006) 및 EPA (2006)의 평가 결과와 일치한다. 선행연구에서도 terbufos의 주요 대사체가 sulfoxide와 sulfone이며, 이들이 식물체 내 전이 과정에서 상대적으로 안정적으로 잔류한다는 점이 보고된 바 있다. 특히 본 연구에서 5배 처리 시 뿌리보다 줄기와 잎에서 총잔류량이 더 높게 나타난 것은 terbufos 산화대사체가 토양에서 식물체로 흡수된 후 지상부로 이행·축적되는 경향을 보여준 기존 연구 결과(Chapman et al., 1982; Szeto et al., 1986)와 부합한다. EPA (2006) 자료에서도 sulfoxide와 sulfone이 terbufos에 비해 토양 흡착계수(Kd)가 낮고 반감기(DT50)가 길어 토양 내 이동성과 지속성이 크다고 보고하고 있어, 본 연구의 결과를 뒷받침한다. 또한 잔류허용기준(maximum residual limit, MRL) 해석과 관련해 미국 및 일부 국가에서는 terbufos 모화합물뿐만 아니라 sulfoxide와 sulfone을 합산하여 총잔류량으로 규제하는 경우가 보고되었다. 본 연구에서 5배 처리구의 결과에서 모화합물보다 대사체의 비중이 훨씬 크게 나타난 점은 이러한 규제 해석 관점과도 일치한다. 따라서 terbufos의 잔류 특성을 평가할 때는 모화합물뿐 아니라 주요 대사체를 포함한 총잔류량으로 해석하는 것이 타당하다.
통계분석 결과, 대파의 경우 처리 수준과 부위에 따른 잔류량에서 모두 유의한 차이가 확인되었으며(p < 0.001), 처리와 부위 간 상호작용 효과 또한 유의하게 나타났다(p < 0.001). Tukey 사후검정 결과, 무처리·1×·5× 처리구 간에는 모두 유의한 차이가 있었고, 특히 5× 처리구에서 줄기와 잎의 잔류량이 뚜렷하게 높았다. t-test에서도 줄기의 terbufos sulfoxide (p = 0.0095)와 잎의 terbufos sulfone (p = 0.0060)이 1× 처리보다 5× 처리에서 유의적으로 높게 검출되었다.
본 연구에서 sulfoxide와 sulfone이 모화합물보다 장기간 잔류한 것은 화학적 안정성 및 환경 상호작용에서 기인한다. 우선, 이들 산화대사체는 terbufos보다 구조적으로 안정하며, 토양 내 관찰적 반감기(DT50)가 terbufos보다 현저히 길게 나타난 것으로 보고되었다(EPA, 2015). 또한 sulfoxide/sulfone은 terbufos보다 토양흡착계수(Kd)가 낮고, 이동성이 커 장기 장외 잔류 및 작물 전이에 기여할 가능성이 크다(EPA, 2015). 토양 유형, 수분 및 유기물 함량이 terbufos 및 그 대사체의 잔류성과 이동성에 중요한 영향을 미친다는 사실도 밝혀졌다(Sarker et al., 2023). 특히 이 연구에서는 phorate와 terbufos 산화체가 주로 토양 상단층(0 - 10 cm)에 집중 분포되며, 유기물 처리 여부에 따라 분해 반감기가 달라졌다(Sarker et al., 2023). 따라서 본 연구에서 관찰된 sulfoxide/sulfone의 장기 잔류성은 단순한 농도 차이가 아니라, 화학적 안정성, 낮은 흡착성·이동성, 토양·환경 조건의 복합적 상호작용에 기반한 결과임을 시사한다. 향후 직접적인 spike-metabolite 처리실험 등을 통해 각 요인의 기여도를 정량화할 필요가 있다.
Table 9.
Residual analysis results for Welsh onion samples of terbufos and its metabolites (mg·kg-1).
| Application | Compound | Root | Pseudostem | Leaf |
| Control | Terbufos | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos oxon sulfone | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos oxon sulfoxide | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos sulfone | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos sulfoxide | < 0.01 | < 0.01 | < 0.01 | |
| Total terbufos residuesz | < 0.01 | < 0.01 | < 0.01 | |
| Recommended dose | Terbufos | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos oxon sulfone | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos oxon sulfoxide | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos sulfone | < 0.01 | < 0.01 | 0.013 | |
| Terbufos sulfoxide | < 0.01 | 0.011 | 0.011 | |
| Total terbufos residuesz | < 0.01 | 0.010 | 0.022 | |
| 5× treatment dose | Terbufos | 0.013 | 0.021 | 0.014 |
| Terbufos oxon | < 0.01 | < 0.01 | < 0.01 | |
| Terbufos oxon sulfone | < 0.01 | 0.023 | 0.019 | |
| Terbufos oxon sulfoxide | 0.013 | 0.027 | 0.023 | |
| Terbufos sulfone | 0.063 | 0.082 | 0.072 | |
| Terbufos sulfoxide | 0.052 | 0.073 | 0.065 | |
| Total terbufos residuesz | 0.132 | 0.213 | 0.181 |
z Terbufos total residues = Terbufos residue + (Terbufos oxon residue ×1.059) + (Terbufos oxon sulfone residue × 0.947) + (Terbufos oxon sulfoxide residue × 1.000) + (Terbufos sulfone residue × 0.900) + (Terbufos sulfoxide residue × 0.947)
• 1.059 = Terbufos molecular weight (288.4) / Terbufos oxon molecular weight (272.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos oxon sulfone molecular weight (304.4)
• 1.000 = Terbufos molecular weight (288.4) / Terbufos oxon sulfoxide molecular weight (288.4)
• 0.900 = Terbufos molecular weight (288.4) / Terbufos sulfone molecular weight (320.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos sulfoxide molecular weight (304.4)
후작물 머위 중 terbufos의 잔류량
Terbufos 3% 입재 희석액을 6 kg·10a-1의 살포물량으로 토양 살포하였을때 후작물 머위 중 terbufos의 잔류량(decline)은 포장 1 (1배수)에서 LOQ 미만, 포장 2 (5배수)에서 0.036 - 0.051 mg·kg-1이었다.
후작물인 머위는 약제 살포 후 40일차부터 10일 간격으로 총 4회 채취하여 잔류량을 조사하였다. 기준량 처리구의 머위 중 terbufos 및 terbufos 산화 대사물의 잔류량은 40일차부터 70일차까지 LOQ 미만이었고 5배량 처리구에서는 0.015 - 0.016 mg·kg-1 잔류하였다. 즉, 전작물 재배 시 살포된 terbufos는 후작물로 재배된 머위로 흡수이행 되는 것으로 나타났다. 비록 아주 미량이지만 비의도적으로 오염되었다고 할 수 있다. 현재 국내에 설정된 머위 중 terbufos의 허용물질목록관리제도(Positive List System, PLS)인 0.01 mg·kg-1을 기준량 처리구에서는 초과되지 않았고 및 5배량 처리구에서는 초과되었다(Table 10). 토양에 terbufos를 처리한 결과 식물 조직에서 terbufos sulfoxide, terbufos sulfone 등 산화대사물이 검출되었다는 보고가 있으며, 현대의 다성분 분석법(LC-MS/MS, QuEChERS 기반 전처리 등)을 통해 이러한 대사물의 검출·정량이 반복 확인되고 있다(Szeto et al., 1986; FAO and WHO, 2006).
머위의 경우, ANOVA 결과 처리 수준과 시기 모두에서 유의한 차이가 확인되었으며(p < 0.001), 5× 처리구에서는 40일차 이후에도 terbufos 및 대사체가 지속적으로 검출되었다. 특히 50일차 이후 5× 처리구의 잔류량은 1× 처리구에 비해 통계적으로 유의하게 높았다(p < 0.05). 머위의 경우에도 처리 수준과 시기에 따른 유의한 차이가 확인되었다.
Table 10.
Residual analysis results for butterbur samples of terbufos and metabolites (mg·kg-1).
| Compound | Recommended dose | 5× treatment dose | ||||||||
| DALA | Control | 40 | 50 | 60 | 70 | Control | 40 | 50 | 60 | 70 |
| Terbufos | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.015 | 0.016 |
| Terbufos oxon | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon sulfone | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.011 | < 0.01 |
| Terbufos oxon sulfoxide | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.012 | < 0.01 | < 0.01 |
| Terbufos sulfone | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.012 | 0.011 | 0.016 |
| Terbufos sulfoxide | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.014 | 0.015 | 0.022 |
| Total terbufos residuesz | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.036 | 0.050 | 0.051 |
z Terbufos total residues = Terbufos residue + (Terbufos oxon residue ×1.059) + (Terbufos oxon sulfone residue × 0.947) + (Terbufos oxon sulfoxide residue × 1.000) + (Terbufos sulfone residue × 0.900) + (Terbufos sulfoxide residue × 0.947)
• 1.059 = Terbufos molecular weight (288.4) / Terbufos oxon molecular weight (272.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos oxon sulfone molecular weight (304.4)
• 1.000 = Terbufos molecular weight (288.4) / Terbufos oxon sulfoxide molecular weight (288.4)
• 0.900 = Terbufos molecular weight (288.4) / Terbufos sulfone molecular weight (320.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos sulfoxide molecular weight (304.4)
토양분석
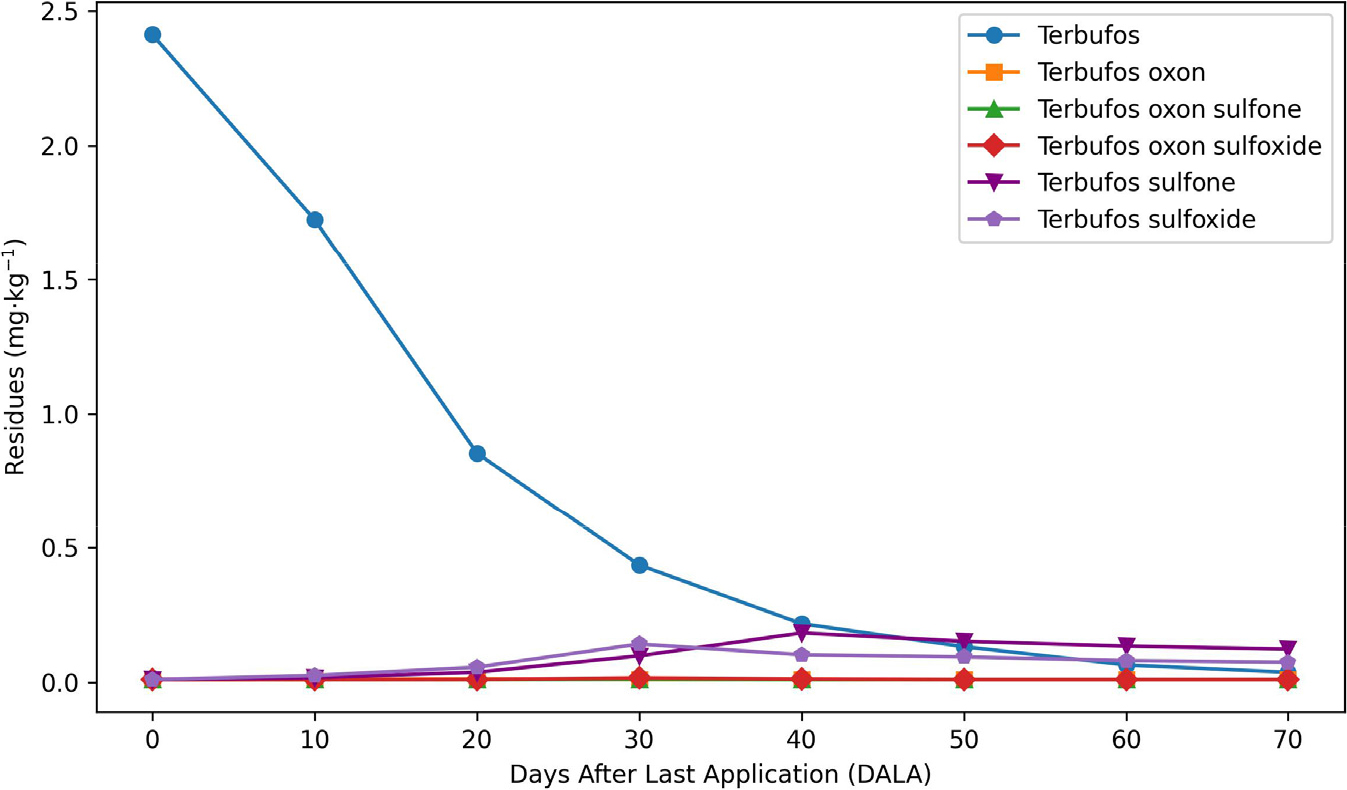
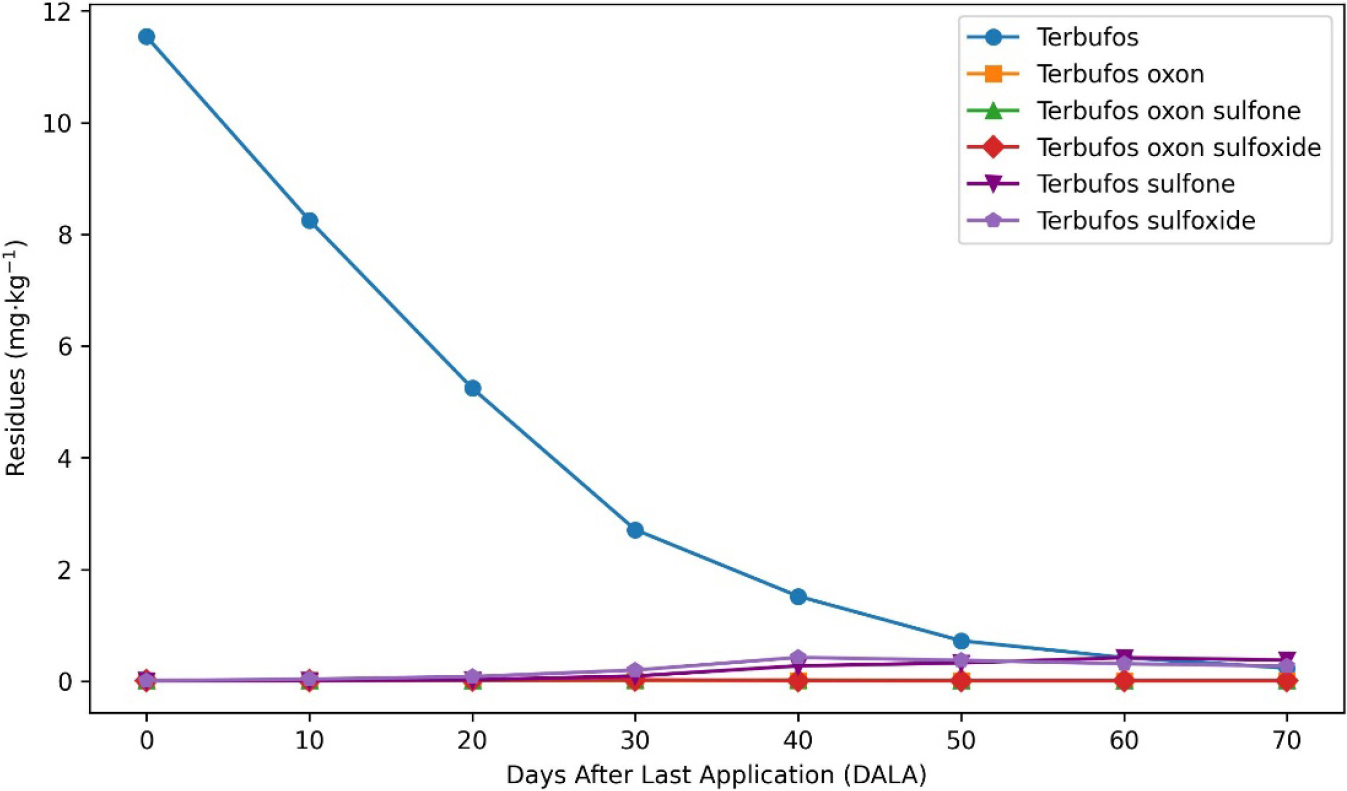
Terbufos 3% 입재 희석액을 6 kg·10a-1의 살포물량으로 토양 살포하였을 때 terbufos 및 산화 대사물 합은 전작물 대파를 파종한 후 기준량 처리의 경우 초기 잔류량은 2.413 mg·kg-1, 5배 처리구의 경우 잔류량은 11.542 mg·kg-1이었다. 시간이 지난 후 토양 중 초기 잔류량은 기준량 처리구에서 71.7% 감소하여 0.684 mg·kg-1, 5배 처리구에서 73.7% 감소하여 3.034 mg·kg-1 잔류되는 것으로 나타났다. 시간에 따른 토양 중 terbufos의 잔류량 변화는 기준량 처리구에 대해 y = 4.8052e-0.584x로 결정계수(R2)가 0.979이었다. 또한, 5배량 처리구에 대한 감소회귀식은 y = 20.132e-0.48x로 도출되었으며 R2은 0.9774로 나타났다. 전작물 재배 기간 동안 terbufos 및 산화대사물의 합의 토양 중 관찰적(observed) 반감기는 기준량 처리구에서 16.5일, 5배수 처리구에서 15.6일로 산출되어 5배 처리구에서 반감기가 더 긴 것으로 나타났다.
후작물 머위는 전작물 수확 후 10일후에 파종하였고 첫 살포일 기준 40일차의 토양중 terbufos와 산화 대사물합의 잔류량은 기준량 처리구에 0.490 mg·kg-1, 5배수 처리구에 2.203 mg·kg-1 이였다. 후작물인 머위를 재배하는 동안 토양 중 terbufos는 기준량 처리구에서 55.5%, 5배량 처리구에서 62.2% 감소하였으며, 머위의 최종 수확일에는 0.218 및 0.833 mg·kg-1 잔류하는 것으로 나타났다. Terbufos의 토양 중에서의 기준량(y = 0.4099e-0.603x, R = 0.9952)과 5배량(y = 2.6697e-0.614x, R2 = 0.9951)에 대해 감소회귀식 및 결정계수를 도출하였다. 후작물 재배 기간 중 토양 중 terbufos 및 산화대사물의 합의 관찰적 반감기는 기준량 처리구에서 25.6일, 5배량 처리구에서 21.3일로 산출되었다(Figs. 1 and 2; Table 11). 이 반감기는 Silt loam토양에서 반감기 21일 연구(Wilson et al., 2002)와 28일후 감소율 62%, 84%의 연구(Ahmad et al., 1979)와 유사하다고 볼 수 있다.
Table 11.
Residual analysis results for soil samples of terbufos and metabolites (mg·kg-1).
| Site 1 | |||||||||
| DALA | Control | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| Terbufos | < 0.01 | 2.413 | 1.725 | 0.854 | 0.435 | 0.217 | 0.132 | 0.064 | 0.037 |
| Terbufos oxon | < 0.01 | < 0.01 | < 0.01 | 0.013 | < 0.01 | < 0.01 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon sulfone | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.011 | < 0.01 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon sulfoxide | < 0.01 | < 0.01 | < 0.01 | < 0.01 | 0.016 | 0.012 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos sulfone | < 0.01 | < 0.01 | 0.017 | 0.037 | 0.098 | 0.183 | 0.152 | 0.134 | 0.123 |
| Terbufos sulfoxide | < 0.01 | < 0.01 | 0.025 | 0.056 | 0.142 | 0.102 | 0.094 | 0.080 | 0.074 |
| Total terbufos residuesz | < 0.01 | 2.413 | 1.764 | 0.954 | 0.684 | 0.490 | 0.358 | 0.260 | 0.218 |
| Site 2 | |||||||||
| DALA | Control | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| Terbufos | < 0.01 | 11.542 | 8.251 | 5.244 | 2.712 | 1.521 | 0.724 | 0.421 | 0.235 |
| Terbufos oxon | < 0.01 | < 0.01 | 0.017 | 0.013 | 0.011 | < 0.01 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon sulfone | < 0.01 | < 0.01 | < 0.01 | 0.011 | 0.017 | 0.022 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos oxon sulfoxide | < 0.01 | < 0.01 | < 0.01 | 0.018 | 0.024 | 0.012 | < 0.01 | < 0.01 | < 0.01 |
| Terbufos sulfone | < 0.01 | < 0.01 | 0.013 | 0.024 | 0.092 | 0.274 | 0.328 | 0.421 | 0.377 |
| Terbufos sulfoxide | < 0.01 | < 0.01 | 0.037 | 0.082 | 0.198 | 0.425 | 0.374 | 0.312 | 0.273 |
| Total terbufos residuesz | < 0.01 | 11.542 | 8.316 | 5.385 | 3.034 | 2.203 | 1.373 | 1.095 | 0.833 |
z Terbufos total residues = Terbufos residue + (Terbufos oxon residue ×1.059) + (Terbufos oxon sulfone residue × 0.947) + (Terbufos oxon sulfoxide residue × 1.000) + (Terbufos sulfone residue × 0.900) + (Terbufos sulfoxide residue × 0.947)
• 1.059 = Terbufos molecular weight (288.4) / Terbufos oxon molecular weight (272.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos oxon sulfone molecular weight (304.4)
• 1.000 = Terbufos molecular weight (288.4) / Terbufos oxon sulfoxide molecular weight (288.4)
• 0.900 = Terbufos molecular weight (288.4) / Terbufos sulfone molecular weight (320.4)
• 0.947 = Terbufos molecular weight (288.4) / Terbufos sulfoxide molecular weight (304.4)
총 재배 기간 중 terbufos의 관찰적 반감기는 기준량 처리구에서 11.6일 5배 처리구에서 12.5일로 산출되었다. Terbufos sulfone, terbufos sulfoxide의 최고 농도 대비 관찰적 반감기는 기준량 처리구에서 52.3일, 42.5일이었고, 5배량 처리구에서 62.8일, 47.0일이었다. 이는 산화 대사체가 모화합물보다 오랜 기간 잔류한다는 보고서(FAO and WHO, 2006; EPA, 2015)와도 유사하다고 볼 수 있다. 추가로 terbufos는 토양에서 지속될 수 있으며, 그 과정에서 점진적으로 sulfoxide와 sulfone으로 변환된다는 연구 결과(Bowman and Sans, 1982; Chapman et al., 1982)와 유사하다고 볼 수 있다.
토양에서도 처리 수준과 시기에 따른 차이가 유의하게 나타났으며(p < 0.001), 처리와 시기 간 상호작용 효과 역시 통계적으로 유의하였다. 다만, 초기 시점에서의 1× 처리구와 5× 처리구 간 차이는 크지만 반복 수가 적어 통계적으로는 뚜렷하지 않았다(p > 0.05).
본 연구에서 산출된 대사체의 반감기는 대사체 자체의 고유(intrinsic) 반감기가 아니라, 모화합물 처리 후 시간 경과에 따른 농도 변화를 기반으로 한 관찰적(observed) 반감기임을 밝힌다. 대사체의 고유한 분해속도를 규명하기 위해서는 해당 대사체를 토양에 직접 처리하는 스파이크 실험과 같은 별도의 연구가 필요하다. 그럼에도 불구하고 본 연구에서 모화합물과 대사체의 반감기를 비교한 이유는, 모화합물이 상대적으로 빠르게 분해되는 반면 대사체는 토양에 더 장기간 잔류할 수 있음을 보여주기 위함이며, 이러한 결과는 환경 잔류 및 식품 안전성 평가 측면에서 중요한 의미를 갖는다.
Conclusion
본 연구는 토양살충제 terbufos를 기준량 및 5배량으로 토양에 처리한 후, 전작물인 대파와 후작물인 머위, 그리고 토양에서의 잔류양상을 통합적으로 분석한 시험으로 의의가 있다. 대파의 경우 기준량 처리 시 30일차에 뿌리에서 총잔류량은 LOQ 미만이었으며, 줄기에서는 terbufos sulfoxide가 0.011 mg·kg-1, 잎에서는 terbufos sulfone과 sulfoxide가 각각 0.013, 0.011 mg·kg-1 검출되었다. 머위는 기준량 처리 시 모든 부위에서 terbufos 총잔류량이 LOQ 미만이었다. 그러나 5배량 처리 시 대파 뿌리에서 terbufos, terbufos oxon sulfoxide, sulfone, sulfoxide가 각각 0.013, 0.013, 0.063, 0.052 mg·kg-1, 줄기에서 0.021, 0.023, 0.027, 0.082, 0.073 mg·kg-1, 잎에서 0.014, 0.019, 0.023, 0.072, 0.065 mg·kg-1 검출되었다. 후작물인 머위에서는 5배량 처리 시 terbufos, sulfone, sulfoxide가 각각 0.016, 0.016, 0.022 mg·kg-1 나타났다.
토양 분석 결과, terbufos 모화합물은 시간 경과에 따라 급격히 감소하였으나, terbufos oxon, terbufos oxon sulfone, terbufos oxon sulfoxide는 10 - 40일차까지 검출되었고, sulfone과 sulfoxide는 30 - 60일차에 최대치를 보인 후 서서히 감소하였다. 특히 sulfone과 sulfoxide의 반감기는 모화합물보다 길어 안정성이 높은 것으로 나타났다.
이러한 결과는 FAO and WHO (2006), EPA (2006) 등 선행연구에서 보고된 바와 같이, terbufos의 주요 잔류형이 sulfoxide와 sulfone이며, 이들이 모화합물보다 안정하고 장기간 잔류한다는 기존 결과와 일치한다. 또한, FAO and WHO (2009) 보고서에서는 일부 농약이 토양에서 분해된 후 대사체 형태로 후작물에 흡수될 수 있음을 언급하고 있으며, 본 연구에서 후작물인 머위에서 대사체가 검출된 것은 이러한 메커니즘을 실증적으로 뒷받침한다. 더불어, 국내외 선행연구에서 보고된 바와 동일하게 기준량 사용 시 terbufos의 총잔류량은 모두 현행 MRL (대파 terbufos 0.05 mg·kg-1, 머위 PLS 0.01 mg·kg-1)보다 낮았고, 5배량 처리 시 농약 기준치를 초과하는 경우도 관찰되었다(RDA 2018).
따라서 terbufos는 기준량 사용 시 현행 MRL 이내로 안전성이 확보되지만, 5배량 처리 시 주요 대사체가 기준치를 초과할 가능성이 있어 토양·작물 안전성 관리에 있어 총잔류량 기준 적용 및 산화대사체에 대한 지속적인 모니터링이 필요하다. 본 연구의 관찰 결과는 토양-작물 전이의 메커니즘을 생리학적 관점에서 설명할 필요성을 제기한다. 특히 토양 및 식물체 내에서의 산화(미생물·화학적·식물 대사)에 의해 형성된 sulfoxide·sulfone 계열의 대사체는 모화합물(parent compound)보다 상대적으로 친수성이 커져 토양 용액에서의 가용성이 증가하고, 증산에 의해 유도되는 목부(xylem) 흐름을 통해 지상부(줄기·잎)로 효율적으로 전이·축적될 수 있다. 이러한 체내 대사 및 격리(sequestration) 과정은 모화합물의 빠른 감소와 대사체의 상대적 장기 잔류를 설명하며, 본 연구의 결과가 보고한 전이·축적 패턴을 뒷받침한다. 따라서 본 메커니즘을 확증하기 위해서는 목부·체관 수액 분석(xylem/phloem sap analysis), 동위원소 추적(stable/radioisotope tracing), 및 수경(hydroponic) 흡수시험 등의 실험적 접근이 병행되어야 한다(Bowman and Sans, 1982; FAO and WHO, 2006; Elsner and Imfeld, 2016; Xia et al., 2024). 본 연구는 전작물-후작물-토양을 연계한 통합 분석을 통해 작물 전환 상황에서의 잔류 특성을 규명하고, 농약 안전관리 정책 수립에 실질적인 근거를 제공하였다.