Introduction
Materials and Methods
실험동물 및 실험 디자인
발효열처리대두박(HFSBM)의 제조 및 사료 급여
착유 대기장 환경 개선처리
실험기간 동안의 온습도지수 분석
유량 및 유성분
혈액 분석
PBMC분리 및 유전자 발현 분석
통계 분석
Results
젖소 고온 스트레스 환경 조건
면역세포 내 고온 스트레스 관련 바이오마커 분석
면역세포 내 염증 관련 유전자 발현
면역세포의 항산화 반응 관련 유전자 발현
고온 스트레스 반응 및 유생산성 변화
생리적 지표
혈액 성상
Discussion
Conclusion
Introduction
지구 온난화로 인한 기후 변화는 전 세계 축산업에 큰 영향을 미치고 있다. 특히 낙농업에서 고능력 개량으로 대사열 발생이 많은 홀스타인 젖소는 고온 스트레스에 매우 취약하다. 고온 스트레스는 젖소의 사료 섭취량 감소, 산유량 저하, 번식 효율 악화, 대사성 질병 증가를 유발하며(West, 2003), 이는 낙농가의 생산성 하락의 주된 원인이 된다. 특히, 고온 환경에 노출된 젖소는 다양한 생리적 변화로 인해 대사가 변화하고 염증 반응이 증가하는 등 면역교란이 발생하여 다양한 질병에 대한 감수성을 높이는 것으로 보고되고 있다(Dahl et al., 2020; Kim et al., 2023).
여름철 젖소의 생산성에 큰 영향을 미치는 고온 스트레스는 개방된 우사에서 뿐 아니라, 착유대기실과 같이 한정된 공간에 다수의 개체가 밀집할 경우 더욱 심화된다. 밀집된 공간에서 젖소에서 발생하는 다량의 대사열과 호흡으로 인한 습기가 원활히 배출되지 못하고 축적되면 내부 온습도지수(temperature humidity index, THI)를 급격히 상승시키고 이는 고온 스트레스를 가중시키는 원인이 된다. 그러므로 젖소 사양 시설환경적 측면에서 착유대기실과 같은 밀집 공간에 환풍기나 송풍팬을 설치하여 공기 흐름을 개선하고 체감온도를 낮추는 것은 효과적인 관리 방법 중 하나일 수 있다(Tresoldi et al., 2018). 하지만 이러한 시설환경 개선 전략은 젖소의 체감 온도를 낮추는 데 기여할 수 있으나, 시설 개선 전략만으로 고온 스트레스로 인한 젖소 체내의 생리적 스트레스 반응을 근본적으로 모두 해결하는 데는 한계가 존재한다. 고온 스트레스는 젖소의 사료 섭취량을 저하시켜 에너지 불균형을 유발 할 뿐 아니라, 체내 호르몬 불균형과 산화 스트레스를 증가시키는 등 다양한 비정상적 대사생리반응을 유도하게된다(West, 2003). 특히, 스트레스 반응으로 인한 단백질 분해 증가와 합성 저하는 젖소의 생산성 및 면역 기능 저하와 직결되는 핵심적인 대사 이상 반응이다(Yue et al., 2020). 그러므로 이러한 고온 스트레스에 노출 된 젖소의 대사 불균형 문제를 완화하기 위한 영양사양적 전략이 요구되며, 그 방법으로 발효 사료와 같은 기능성 원료를 급여하여 소화율을 개선하고 장 건강을 증진시켜 스트레스 저항성을 높이려는 시도도 이루어지고 있다(Al-Qaisi et al., 2020). 특히 발효대두박은 유용미생물을 이용한 발효 과정을 통해 소화 흡수율이 높은 단백질원으로, 다양한 생리활성 기능을 가지는 것으로 알려져 있다(Kim et al., 2012). 또한 대두박에 열처리는 당 알데히드 그룹과 단백질의 유리 아미노산 그룹 사이에 당 복합체를 형성하여 마이야르 반응 또는 비효소 반응 촉진을 통해 반추위에서 단백질과 아미노산의 분해를 줄여 반추위 미분해 단백질(rumen undegradable protein, RUP)을 증가 시킨다고 알려져 있다(Kung and Rode, 1996; ASA, 1999).
현재까지 다양한 고온 스트레스 저감을 위한 시설적 그리고 영양적 전략을 개발하기 위한 연구에도 불구하고, 젖소의 고온 스트레스 저감 효과는 크지 않은 것이 사실이다. 그러므로 낙농가의 시설환경 개선과 기능성 사료 첨가 급여를 복합적으로 적용하여 젖소의 고온 스트레스 저감 효과를 극대화하는 노력이 필요할 것이다. 따라서 본 연구에서는 고온 스트레스 환경에 노출된 홀스타인 젖소를 대상으로 착유대기실 환풍기 설치를 통한 쿨링 시스템 적용과 발효열처리대두박(heat-treated fermented soybean meal, HFSBM) 첨가 급여 동시에 적용하였을 때 젖소의 생산성, 면역 및 세포 스트레스 반응에 미치는 영향을 평가하고자 하였다.
Materials and Methods
실험동물 및 실험 디자인
본 실험은 국립축산과학원 동물실험윤리위원회의 사전 승인(NIAS20250019)하에 수행되었다. 천안에 위치한 국립축산과학원 농장에서 사육 중인 홀스타인 젖소 12두를 대상으로 2주간 진행되었으며, 공시축은 평균 산차(control [CON]: 1.5 ± 0.5, heat stress-mitigating treatment [HSMT]: 1.6 ± 0.6; mean ± standard error of the mean [SEM])와 평균 비유일수(CON: 102.5 ± 223, HSMT: 114.8 ± 45; mean ± SEM)를 고려하여 2개 처리구로 완전 임의 배치하였다. 대조구는 기존 젖소 사양 관리 프로그램을 따르며, 기존의 착유대기장을 사용하여 착유를 진행하였다(CON; n = 6). 고온 스트레스 완화 처리를 적용한 처리구는 추가적인 발효열처리대두박을 급여하였고, 환경 개선처리된 착유대기장을 사용하여 착유를 진행하였다(HSMT; n = 6). 실험 기간 동안 모든 젖소에게 동일한 total mixed ration (TMR)을 급여하였고, 관행적인 착유대기장을 이용하였다. HSMT 그룹은 추가로 급여량의 0.1% HFSBM을 탑 드레싱방식으로 급여하며, 쿨링시스템이 적용된 착유대기장을 이용하였다.
발효열처리대두박(HFSBM)의 제조 및 사료 급여
실험 기간 동안 모든 한 두당 TMR 36.8 kg을 2회(오전, 오후)에 나눠 급여하였다. 물은 상시 접근 가능하도록 하였다. CON 그룹은 한국가축사양표준(NIAS, 2022)의 영양소 요구량에 따라 국립축산과학원에서 제조한 TMR (Table 1)을 급여하였다. 대두박의 발효는 Enterococcus faecium과 Lactobacillus plantarum을 이용하였으며 방법은 다음과 같다. 발효용기에 담긴 대두박 400 g 당 단일 미생물 배양액(1.0 × 108 CFU·mL-1)을 10 mL씩, 총 20 mL를 분무 방식으로 처리하여 37°C에서 48시간 동안 발효시켰다. 이후 130°C에서 45분 동안 열처리 과정을 진행하였다(Yarandi et al., 2016).
Table 1.
Ingredients and chemical composition of diets.
| Items | TMR |
| Ingredients (% DM) | |
| Concentrate | 28.5 |
| Grass hay | 16.3 |
| Timothy hay | 5.4 |
| Alfalfa hay | 5.4 |
| Steamed corn silage | 32.6 |
| Soybean meal | 1.4 |
| Whole cottonseed | 5.4 |
| Beet pulp | 4.1 |
| Mineral and vitamin premixz | 0.6 |
| Total | 100 |
| Chemical composition (g·kg-1 DM) | |
| DM | 684.5 |
| CP | 179.2 |
| EE | 37.8 |
| NDF | 468.9 |
| ADF | 279.9 |
| Ca | 7 |
| P | 4.1 |
착유 대기장 환경 개선처리
CON 그룹은 관행적으로 활용되는 착유대기장을 이용하여 착유를 실시하였으며, HSMT 그룹은 쿨링 시스템(10 × 9 m2)이 적용된 착유대기장을 이용하여 30분간 대기 후 착유를 실시하였다. 쿨링 시스템은 온습도변화에 따라 작동하는 송풍팬과 고압분무장치로 구성되었다. 송풍팬은 직경 1,060 mm로 320 m3·min-1의 풍량을 제공하였고, 고압분무장치는 0.15 mm의 노즐 직경으로 120 L·h-1의 분무량을 제공하였다. 풍량 및 분무량은 고온기 가축사양 및 환경관리 기술지침(NIAS, 2018)의 기준을 토대로 설정하였다.
실험기간 동안의 온습도지수 분석
실험 기간 중 축사 내부 환경 조건을 디지털 온습도계(Testo 625, Testo SE & Co. KGaA, Germany)를 사용하여 실험 1일차, 7일차, 14일차, 총 3번에 걸쳐 측정하고 기록하였으며, 아래의 식(1)에 따라 THI를 산출하였다.
여기서, T는 온도(°C), RH는 상대습도(%)이다.
유량 및 유성분
착유는 텐덤 착유기를 사용하였으며, 착유 후 개체별 유량이 자동 착유 시스템에 기록되었다. 착유 시스템에서 우유 샘플을 채취하여 유성분 분석기(Milkoscan, Foss Technology, Denmark)를 이용해 유지방, 유단백, 유당 및 체세포수를 분석하였다. 착유는 매일 오전 8:00시와 오후 18:00시 2회에 걸쳐 이루어졌다.
혈액 분석
혈액은 실험 시작 후 14일에 실험축의 경정맥을 통해 BD Vacutainer® spray-coated K2EDTA tube (BD Franklin Lakes, USA)와 BD Vacutainer® SST tube (BD Franklin Lakes, USA)를 이용하여 채취하였다. 채혈 직후 튜브는 즉시 얼음 위에 올려져 실험실로 옮겨졌다. SST 튜브는 실온에서 20분간 방치시킨 다음 2,000 × g, 4°C에서 20분간 원심분리하였다. K2EDTA 튜브의 혈액 일부는 즉시 전혈구검사(complete blood count, CBC)분석에 사용되었고 나머지는 말초혈액 단핵세포(peripheral blood mononuclear cells, PBMCs)분리에 사용되었다. 전혈구검사(CBC)는 자동 혈구 분석기(ProCyte Dx, IDEXX, USA)를 이용하였고, 혈액화학 분석은 생화학 분석기(Hitachi 7180, Hitachi, Japan)를 이용하였다.
PBMC분리 및 유전자 발현 분석
PBMC는 밀도구배 원심분리를 사용하여 분리하였다. 전혈 샘플을 phosphate buffered saline (PBS)과 1 : 1비율로 희석하고 희석된 혈액과 Lymphoprep (STEMCELL Technologies Inc., Canada)을 이용해 800 × g, 실온으로 20분 동안 원심분리하였다. 원심분리 후 중간층의 PBMC를 분리하고 새로운 PBS로 세척한 후 유전자 발현 분석 실험을 위해 1 mL의 TRIzol이 들어 있는 튜브로 옮기고 -80°C에서 보관하였다. 유전자 발현 분석 실험은 PBMC샘플에서 총 RNA를 추출하고 특정 프라이머를 사용하여 유전자의 mRNA 발현 수준을 평가하였다. 간략하게 설명하면 분리한 PBMC가 담겨 보관되어 있는 TRIzol을 실온에서 해동하고 200 uL의 클로로포름을 첨가하였다. 이후 15초 동안 볼텍싱하여 혼합시키고 실온에서 3분 동안 방치하였다. 이후 샘플을 10,000 × g, 4°C에서 20분간 원심분리하였다. 상층액을 500 uL의 이소프로필 알코올이 들어 있는 새 튜브로 옮기고 부드럽게 볼텍싱하여 혼합하였다. 이를 실온에서 10분 동안 방치한 후 혼합물을 10,000 × g, 4°C에서 10분간 원심분리하였다. 상층액을 버리고 펠릿을 75% diethyl pyrocarbonate (DEPC) 에탄올로 세척하고 건조한 후 DEPC water (Invitrogen, USA)에 보관하였다. cDNA는 AccuPower RT PreMix (Bioneer, Korea)를 사용하여 합성하였다. qRT-PCR은 QuantStudio 1 (Applied Biosystems, USA)및 SolgTM h-Taq DNA Polymerase (SolGent, Korea)를 사용하여 수행하였다. qRT-PCR은 50°C에서 10분, 95°C에서 5분, 그 이후 95°C 15초와 60°C 30초의 사이클을 40반복하여 수행하였다. mRNA발현 수준은 하우스키핑 유전자인 β-actin을 이용하여 상대적으로 평가하였다(Eom et al., 2025). qRT-PCR에서 사용한 프라이머는 Table 2에 나타내었다.
Table 2.
Sequence of the primers used for qRT-PCR analysis.
β-actin, beta-actin; IL-1β, interleukin-1 beta; IL-2, interleukin-2; IL-6, interleukin-6; IL-10, interleukin-10; IL-17A, interleukin-17A; INF-γ, interferon-gamma; TNF-α, tumor necrosis factor-alpha; HSP70, heat shock protein 70; HSP90, heat shock protein 90; GSR, gluitathione reductase; SOD1, superoxide dismutase 1; CAT, catalase.
통계 분석
생체지표 통계분석은 R 소프트웨어 4.5.1 (R Core Team, 2025)을 사용하여 수행하였다. 각 측정항목에 대해 두 그룹 간 평균차이를 비교하기 위해 독립 표본 t-검정(independent samples t-test)을 실시하였다. mRNA 발현량 데이터 통계 분석은 Prism 소프트웨어 8.0 (GraphPad, 2018)을 사용하여 정규성을 검정하였으며 정규 분포를 따르는 데이터는 독립 표본 t-검정을, 정규 분포가 아닌 데이터는 Mann-Whitney test를 이용하여 분석하였다. 모든 데이터의 통계적 유의성은 p < 0.05 수준에서 판단하였으며, 0.05 ≤ p < 0.10 범위의 p 값은 통계적 경향성으로 정의하여 논의하였다.
Results
젖소 고온 스트레스 환경 조건
본 실험 기간 동안 동물의 사육 공간에서 1일, 7일, 14일에 THI 지수를 측정하였고 실험기간동안 평균 THI 지수는 80.60 (SEM: 0.93)으로 나타났다. 일반적으로 젖소의 적정 온습도 지수는 68 미만으로 간주되며, 72부터 고온 스트레스가 시작된다고 보고되어 있다(Armstrong, 1994). 따라서 본 동물실험은 고온 스트레스 환경 조건에서 수행되었음을 확인하였다. 쿨링 시설 가동 시 착유 대기장의 온도는 평균 0.5도가 저감되었으며 풍량은 평균 0.2 m3·min-1 만큼 증가하였다.
면역세포 내 고온 스트레스 관련 바이오마커 분석
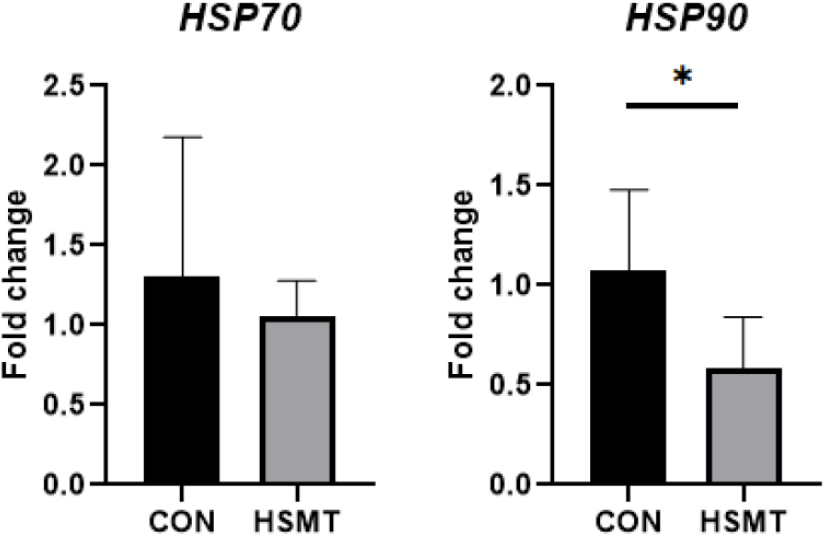
고온 스트레스에 노출된 젖소의 PBMC에서 열충격 단백질 유전자 발현 수준 분석을 통해 고온 스트레스 완화처리(HSMT)의 효과를 확인하였다(Fig. 1). HSP70의 유전자 발현은 CON 그룹과 HSMT 그룹 간에 통계적으로 유의미한 차이를 보이지 않았다. 반면, HSP90의 유전자 발현은 CON 그룹과 비교하여 HSMT 그룹에서 통계적으로 유의하게 감소하였다(p = 0.027).
면역세포 내 염증 관련 유전자 발현
고온 스트레스에 노출된 PBMC의 염증 관련 사이토카인 유전자 발현 수준을 통해 고온 스트레스 완화처리(HSMT)의 효과를 확인하였다(Fig. 2). 주요 염증성 사이토카인인 IL-1β의 유전자 발현은 CON 그룹 대비 HSMT 그룹에서 유의하게 감소하였다(p = 0.038). 마찬가지로 INF-γ의 유전자 발현 또한 CON 그룹과 비교하여 HSMT 그룹에서 유의하게 억제되었다(p = 0.021). IL-2, IL-6, TNF-a와 같은 다른 염증성 사이토카인의 발현은 HSMT 그룹에서 감소하는 경향(각 p = 0.072, p = 0.075, p = 0.064)이 관찰되었으나, 통계적 유의차에는 도달하지 못하였다.
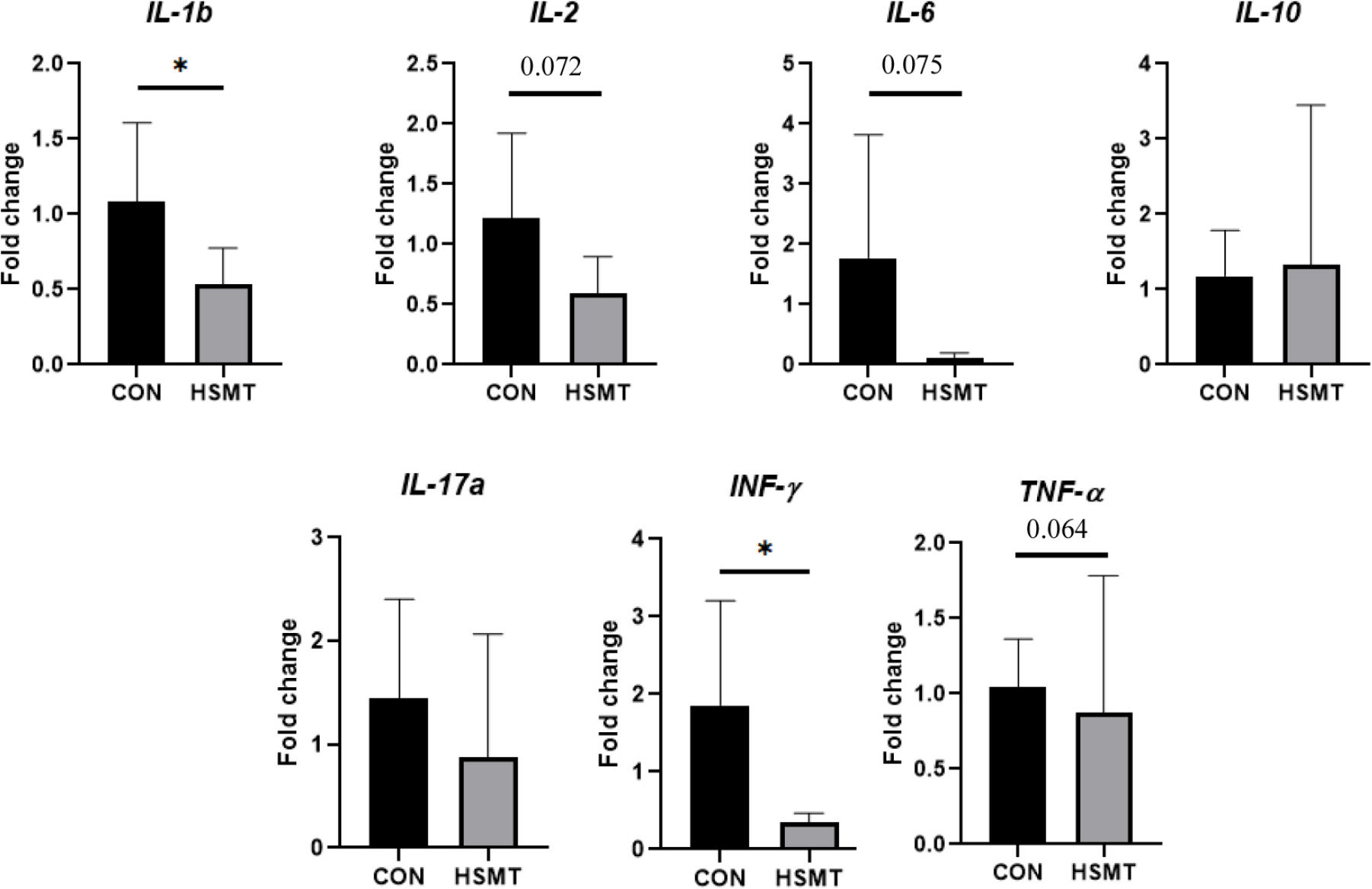
Fig. 2.
Effect of heat stress mitigation treatment (HSMT) on pro-inflammatory cytokine gene expression in heat-stressed peripheral blood mononuclear cells (PBMCs). CON, control; IL, interleukin; INF, interferon; TNF, tumor necrosis factor. The bars indicate means ± standard deviation (SD). * p < 0.05.
면역세포의 항산화 반응 관련 유전자 발현
고온스트레스에 노출된 PBMC의 항산화 유전자 발현 수준 분석을 통해 고온 스트레스 완화처리(HSMT)의 효과를 확인하였다(Fig. 3). HSMT 그룹은 CON 그룹과 비교하여 주요 항산화 효소인 SOD1과 CAT의 유전자 발현이 유의하게 증가하였다(각 p = 0.003, p = 0.002). GSR의 유전자 발현은 두 그룹 간의 통계적으로 유의미한 차이는 발견되지 않았다.
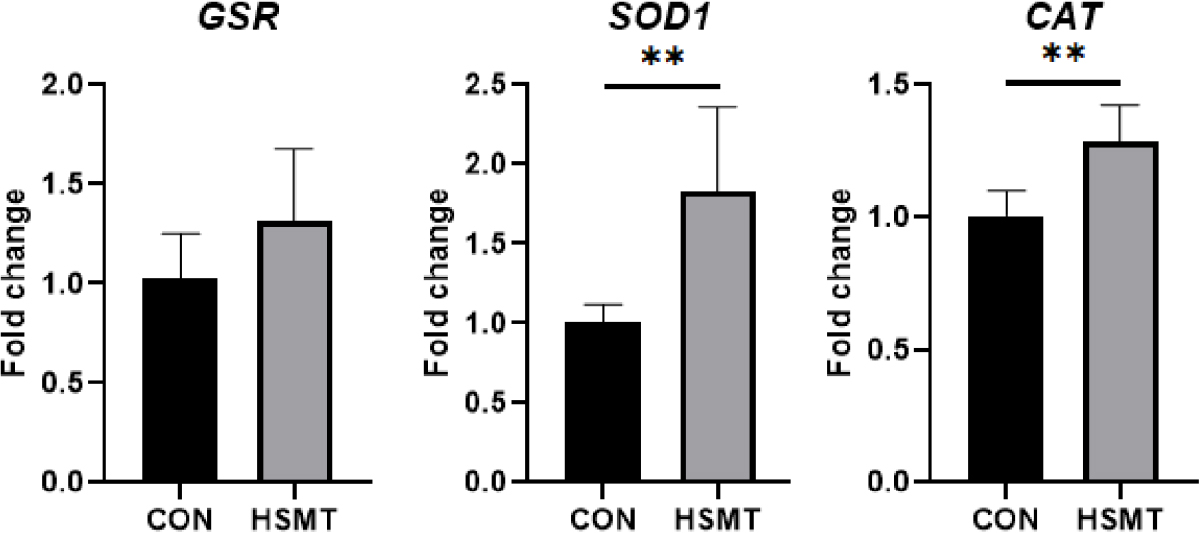
Fig. 3.
Effect of heat stress mitigation treatment (HSMT) on the gene expression of antioxidant enzymes in heat-stressed peripheral blood mononuclear cells (PBMCs). CON, control; GSR, glutathione reductase; SOD, superoxide dismutase; CAT, catalase. The bars indicate means ± standard deviation (SD). ** p < 0.01.
고온 스트레스 반응 및 유생산성 변화
HSMT가 젖소의 우유 생산성 및 품질에 미치는 영향을 평가하였다. HSMT는 젖소의 유생산량과 우유 내 단백질 및 지방 함량에 영향을 미치지는 않았다. 우유 성분 중 우유의 품질 지표인 체세포 수(somatic cell count)는 HSMT 그룹에서 낮은 수치를 기록하였으나, 통계적인 유의성이나 경향성은 관찰되지 않았다(Table 3).
Table 3.
Effect of cooling system operation and heat-treated fermented soybean meal supplementation on milk yield and composition of Holstein dairy cows in heat stress condition.
생리적 지표
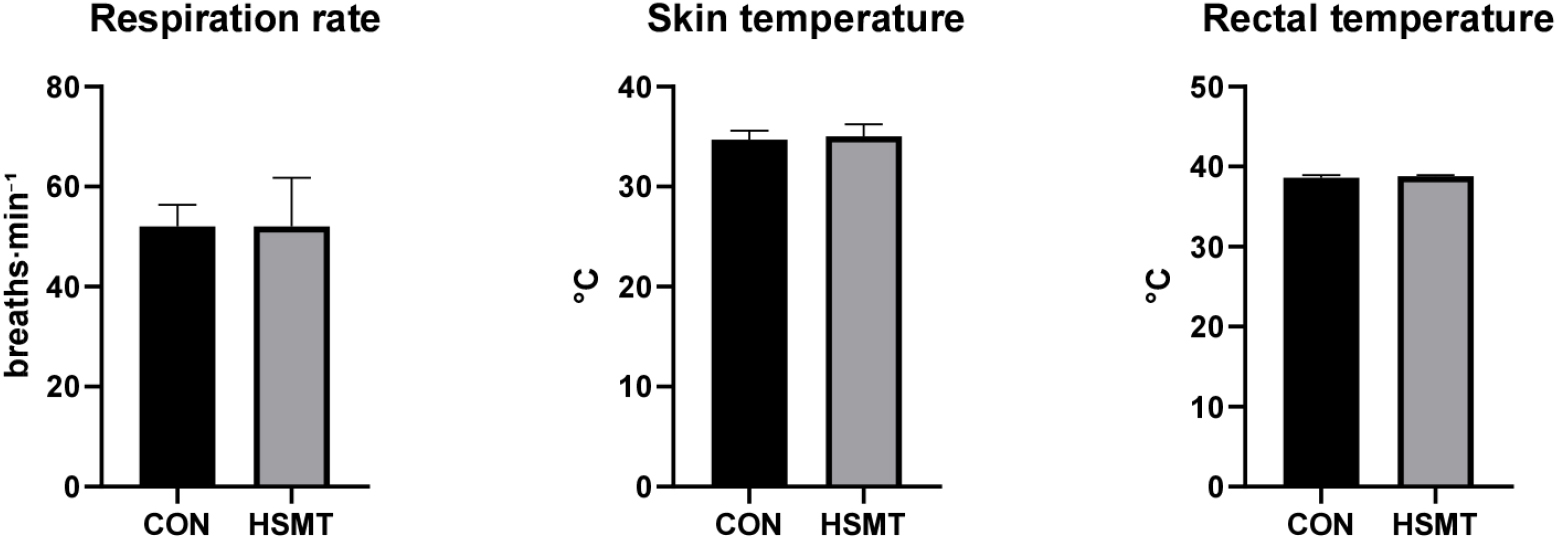
고온 스트레스 완화 처리가 젖소의 생리적 스트레스 반응 완화에 미치는 영향을 평가하기 위해, 고온 스트레스의 대표적 지표인 호흡수, 체표온도 및 직장 온도를 측정하였다. 하지만, CON 그룹과 HSMT 그룹 간에 유의미한 차이는 발견되지 않았다(Fig. 4).
혈액 성상
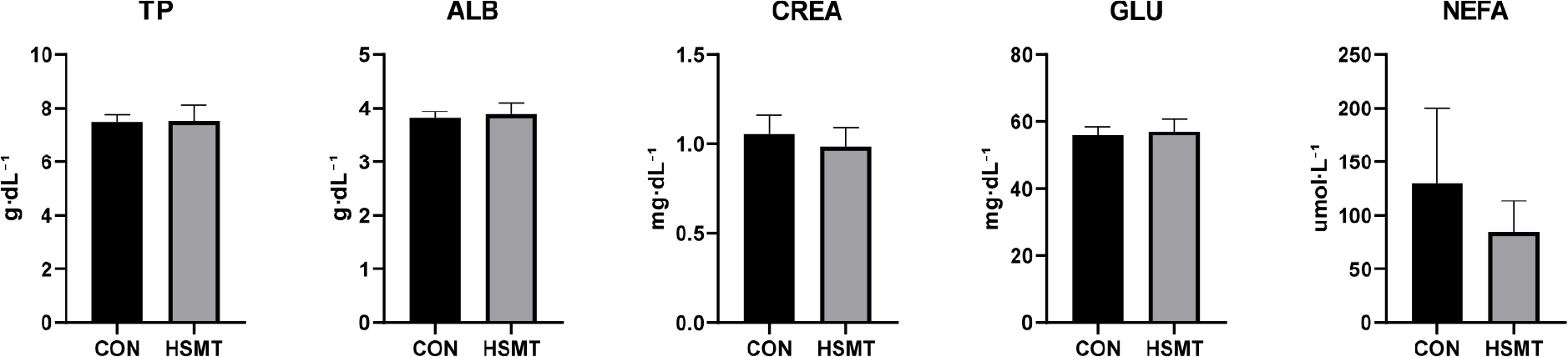
일반 혈액 분석 결과에서는 두 그룹 간 평균적혈구용적(mean corpuscular volume, MCV) 항목에서 유의한 차이를 보여 CON 그룹이 HSMT 그룹 보다 큰 값을 나타내었다(p = 0.04; Table 4). 또한 호기염구(basophil, BA; ×103·µL-1)의 경우 유의한 차이는 없었지만 HSMT 그룹에서 증가하는 경향을 보였다(p = 0.08; Table 4). 하지만 혈액 화학분석에서는 그룹별 유의한 차이는 발견되지 않았다(Fig. 5).
Table 4.
Effect of cooling system operation and heat-treated fermented soybean meal supplementation on blood components of Holstein dairy cows in heat stress condition.
p-values indicate the significance of the treatment effect, where * p < 0.05 was considered statistically significant and 0.05 ≤ p < 0.1 was considered a tendency.
SEM, standard error of the mean; CON, control; HSMT, heat stress-mitigating treatment; RBC, red blood cell; HCT, hematocrit; Hb, hemoglobin; MCV, mean corpuscular volume; MCH, mean corpuscular hemoglobin; MCHC, mean corpuscular hemoglobin concentration; RDW, red cell distribution width; RETIC, reticulocyte; WBC, white blood cell; NE, neutrophil; LY, lymphocyte; MO, monocyte; EO, eosinophil; BA, basophil; PLT, platelet count; MPV, mean platelet volume; PDW, platelet distribution width; PCT, plateletcrit.
Discussion
본 연구는 고온기 홀스타인 젖소에게 HFSBM 급여와 착유대기실 환풍기 적용 시 젖소 고온 스트레스 완화 효과를 평가하였다. 2주간의 실험 기간 동안 고온 스트레스 완화 유도 처리(HSMT)는 산유량, 유성분 등 직접적인 젖소 생산성 지표나 호흡수, 체온과 같은 고온 스트레스 관련 생리 지표에 유의한 변화를 일으키지 않았다. 이는 본 실험 기간이 다소 짧았거나, 공시된 소들의 산유 능력이 아주 높지 않아 고온 스트레스에 대한 반응 임계치에 도달하지 않았을 가능성이 있다. 그러나 분자 수준에서의 면역 및 세포 스트레스 지표 변화는 생산성 지표보다 훨씬 민감하게 반응하여 HSMT의 잠재적 완화 효과를 선제적으로 투영 하고 있다.
고온 스트레스는 혈류를 체표면으로 분산시켜 장관 내 허혈을 초래하며, 이는 장 상피세포의 투과성을 높이는 장 누수 현상을 유발하여 내독소나 항원 단백질의 체내 유입을 촉진한다(Baumgard and Rhoads Jr, 2013). HSMT 그룹에서 전염증성 사이토카인인 IL-1β와 IFN-γ의 발현이 유의하게 감소한 것은 고온 스트레스로 유발되는 전신 염증 상태가 완화되었음을 의미한다(Zhang et al., 2025).
또한 주요 항산화 효소인 SOD1과 CAT의 발현 증가는 주목할 만한 결과이다. 고온 스트레스는 젖소 체내에서 활성산소종(reactive oxygen species, ROS)의 생성을 증가시켜 산화 스트레스를 유발하며, 이는 세포 손상, 면역 기능 저하 및 생산성 감소로 이어지는 주요 원인 중 하나로 알려져 있다(Guo et al., 2021). SOD1은 세포질에서 초과산화물 음이온(superoxide anion)을 과산화수소(H2O2)로 전환시키는 1차 방어 효소이며, CAT는 이렇게 생성된 과산화수소를 물과 산소로 분해하여 무해화 시키는 핵심 효소이다(Ighodaro and Akinloye, 2018). 따라서 HSMT 그룹에서 SOD1과 CAT 수준이 증가했다는 것은, 해당 처리 조건이 젖소에서 고온 스트레스로 인해 증가된 산화 스트레스를 감소시켜 내인성 항산화 방어 시스템을 강화하는 데 기여할 수 있음을 시사한다(Zhang et al., 2025).
항산화 체계의 활성화는 전반적인 세포 내 스트레스 지표의 안정화로 이어진다. 실제로 HSMT 그룹에서 관찰된 HSP90 발현의 유의적인 감소는 고온 스트레스에 노출된 젖소의 실질적인 스트레스 부하가 대조군에 비해 완화되었음을 투영하는 결과이다(Sarma et al., 2025). 일반적으로 열 스트레스 조건에서는 단백질 변성을 막기 위해 HSP 발현이 상향 조절되지만, 본 연구에서의 감소는 물리적 냉각과 HFSBM의 영양학적 지원이 시너지를 일으켜 세포가 HSP90을 과도하게 발현시킬 필요성이 적었음을 시사한다.
이러한 긍정적 변화의 핵심 기전 중 하나는 HFSBM의 독특한 영양학적 가치에 있다. HFSBM은 발효 과정을 통해 단백질이 저분자 펩타이드로 분해되어 면역 조절 기능을 수행할 뿐만 아니라, 정밀한 열처리를 통해 반추위 비분해 단백질(RUP) 수준을 증가시킴으로써 고온기 사료 섭취량 감소 시 부족하기 쉬운 필수 아미노산을 소장에 효율적으로 공급한다(Flis and Wattiaux, 2005). 특히 RUP의 증가는 반추위 내 단백질 분해 후 생성되는 암모니아를 억제하여 요소 합성 과정에서 발생하는 대사열을 완화하는 데 기여할 수 있다. 이러한 내부적인 대사 부하의 감소는 환풍기를 통한 물리적 냉각 효과를 보완하는 상승 요인으로 작용했을 것으로 사료된다. 아울러 HFSBM 내의 이소플라본 역시 미생물 효소에 의해 생물학적 활성이 높은 형태로 변형되어 장벽 기능을 강화하고 세포 내 항산화 시스템을 증진시키는 데 기여한 것으로 판단된다(Do Prado et al., 2022).
또한 본 실험의 처리구에서 유의한 차이는 아니지만, 유리지방산(non-esterified fatty acid, NEFA)의 감소와 글루코스(glucose, GLU)의 상승하는 수치는 에너지 대사가 긍정적으로 개선되었을 가능성을 제시한다(Fig. 4). 특히 NEFA는 체지방 분해의 지표로서 NEFA가 대량으로 발생하면 간에 축적되어 지방간을 유발하고, 불완전하게 대사되면서 케톤체를 생성시켜 케토시스를 유발하기도 한다. 즉 NEFA가 낮아진 것은 대사 질병의 위험이 낮아졌음을 의미한다(Caixeta and Omontese, 2021).
본 연구는 영양적 처리와 시설환경적 처리의 복합 처리 효과를 보기 위해 디자인되었다. 이는 여름철 젖소의 고온 스트레스 완화 효과를 극대화하기 위함이며, 또한 많은 낙농가에서 실제로 시설 환경적 개선과 영양사료적 접근을 동시에 적용하고자 함을 고려한 것이다. 다만 복합 처리 조건에서 관찰된 다양한 고온 스트레스 반응 저감 효과들이 어떤 요인으로부터 유발 되었는지 그리고 단일 처리가 아닌 복합 처리 시 시너지 효과를 가지는지에 대한 명확한 결론을 내리기 어려운 한계를 가지고 있다. 따라서 각 요인의 독립적 효과 및 상호작용 효과를 규명하기 위한 후속 연구 진행을 통해 젖소의 고온 스트레스 저감 효과를 극대화하기 위한 노력이 필요할 것이다.
비록 본 실험이 물리적 냉각과 HFSBM 급여의 개별 기여도를 분리하여 분석하지 못한 한계는 있으나, 현장 적용 관점에서는 시설 환경과 사양 관리를 병행하는 복합 모델의 실용적 가치를 입증했다는 점에서 의의가 있다. 다만, 한국의 고온 다습한 여름철 환경에서는 습도가 환풍기의 냉각 효율을 제한할 수 있으므로, 향후 연구에서는 냉각 강도와 RUP 공급 수준간의 상호작용을 정밀하게 규명할 필요가 있다.
Conclusion
고온기 홀스타인 젖소에게 2주간 발효열처리대두박 첨가 급여와 착유대기실 환경 개선을 포함하는 복합 스트레스 완화 처리(HSMT)를 적용한 결과, 유량, 유질 및 생리적 지표에는 유의한 영향을 미치지 않았으나, 젖소 PBMC 내 염증성 사이토카인(IL-1β, IFN-γ)과 세포 스트레스 지표(HSP90) 유전자의 발현을 유의하게 감소시켜, 해당 처리가 분자 수준에서 젖소의 고온 스트레스 완화에 효과가 있음을 확인하였다. 이는 고온 스트레스 저감을 위해 착유장 환경 개선과 기능성 사료의 동시적용은 젖소의 스트레스 반응을 저감 시키고 건강을 유지하는데 기여할 수 있음을 제시한다.